
【题目】有甲、乙两醋酸稀溶液,测得甲的pH=a,乙的pH=a+1.下列推断中正确的是( )
A.物质的量浓度c(甲)=10c(乙)
B.甲中由水电离产生的H+的物质的量浓度和乙的相等
C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)>10V(甲)
D.甲中的c(OH﹣)为乙中c(OH﹣)的10倍
【答案】C
【解析】解:A.如果醋酸的电离程度相等,则物质的量浓度c(甲)=10c(乙),实际上乙的电离程度大于甲,所以c(甲)>10c(乙),故A错误;
B.甲中水电离出的氢离子= ![]() ,乙中水电离出的氢离子浓度=
,乙中水电离出的氢离子浓度= ![]() ,所以甲中由水电离产生的H+的物质的量浓度是乙的0.1倍,故B错误;
,所以甲中由水电离产生的H+的物质的量浓度是乙的0.1倍,故B错误;
C.因为c(甲)>10c(乙),所以中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)>10V(甲),故C正确;
D.相同温度下,水的离子积常数相同,根据PH知,甲中氢氧根离子浓度= ![]() ,乙中氢氧根离子浓度=
,乙中氢氧根离子浓度= ![]() ,则甲中氢氧根离子浓度是乙的
,则甲中氢氧根离子浓度是乙的 ![]() ,故D错误;
,故D错误;
故选C.
【考点精析】解答此题的关键在于理解弱电解质在水溶液中的电离平衡的相关知识,掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】燃料电池是一种能量转换效率高、对环境友好的化学电源,如图为一种氢氧燃料电池的结构装置。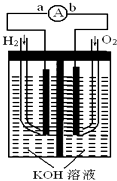
(1)电极b为该燃料电池的极(填“正”或“负”),电极方程式为;
(2)电池工作时,溶液中的OH﹣移向极(填“a”或“b”);
(3)电池工作时,在导线中电子流动方向为(用a、b表示);
(4)电池使用一段时间后,溶液的pH值(填“增大”或“减小”);
(5)当电池工作一段时间后消耗标准状况下H2 为6.72L时,转移电子 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置,写出除去下列物质中的杂质的方法,并写出化学方程式(括号内的气体为杂质). 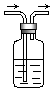
(1)CO2( SO2) , 化学方程式 .
(2)SO2 ( HCl ) , 化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:3CH4(g)+2N2(g)3C(s)+4NH3(g)△H>0,700℃时,CH4与N2在不同物质的量之比[ ![]() ]时CH4的平衡转化率如图所示.下列说法正确的是( )
]时CH4的平衡转化率如图所示.下列说法正确的是( ) 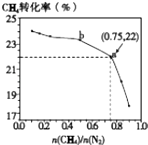
A.![]() 越大,CH4的转化率越高
越大,CH4的转化率越高
B.![]() 不变时,若升温,NH3的体积分数会增大
不变时,若升温,NH3的体积分数会增大
C.b点对应的平衡常数比a点的大
D.a点对应的NH3的体积分数约为26%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素随着原子序数的增大,下列递变规律正确的是
A. 单质熔、沸点逐渐降低B. 单质的氧化性逐渐增强
C. 原子半径逐渐增大D. 气态氢化物稳定性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com