

 ;
; ;
;分析 根据A→B+C(水解反应)可以判断A、B、C分别是酯、羧酸和醇,且由(1)可以确定B和C的结构分别为(CH3)2CHCOOH和(CH3)2CHCH2OH,则D为 (CH3)2C=CH2,由D到E是取代反应,E为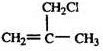 ,E发生水解得到醇F,G为醛且含有双键,可以写出其结构为CH2=C(CH3)-CHO,发生反应⑦得到羧酸H为CH2=C(CH3)-COOH,H与CH3OH得到酯I为CH2=C(CH3)-COOCH3,则J为加聚反应的产物,为
,E发生水解得到醇F,G为醛且含有双键,可以写出其结构为CH2=C(CH3)-CHO,发生反应⑦得到羧酸H为CH2=C(CH3)-COOH,H与CH3OH得到酯I为CH2=C(CH3)-COOCH3,则J为加聚反应的产物,为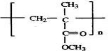 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.
解答 解:根据A→B+C(水解反应)可以判断A、B、C分别是酯、羧酸和醇,且由(1)可以确定B和C的结构分别为(CH3)2CHCOOH和(CH3)2CHCH2OH,则D为 (CH3)2C=CH2,由D到E是取代反应,E为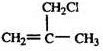 ,E发生水解得到醇F,G为醛且含有双键,可以写出其结构为CH2=C(CH3)-CHO,发生反应⑦得到羧酸H为CH2=C(CH3)-COOH,H与CH3OH得到酯I为CH2=C(CH3)-COOCH3,则J为加聚反应的产物,为
,E发生水解得到醇F,G为醛且含有双键,可以写出其结构为CH2=C(CH3)-CHO,发生反应⑦得到羧酸H为CH2=C(CH3)-COOH,H与CH3OH得到酯I为CH2=C(CH3)-COOCH3,则J为加聚反应的产物,为 ,
,
(1)由以上分析可知B为(CH3)2CHCOOH,故答案为:(CH3)2CHCOOH;
(2)反应⑤为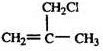 的水解反应,反应的方程式为
的水解反应,反应的方程式为 ,
,
G为CH2=C(CH3)-CHO,发生反应⑦得到羧酸H为CH2=C(CH3)-COOH,反应⑦的化学方程式为CH2=C(CH3)-CHO+2Cu(OH)2$\stackrel{△}{→}$CH2=C(CH3)-COOH+Cu2O↓+2H2O,
反应⑨为CH2=C(CH3)-COOCH3的加聚反应,反应的方程式为 ,
,
故答案为: ;CH2=C(CH3)-CHO+2Cu(OH)2$\stackrel{△}{→}$CH2=C(CH3)-COOH+Cu2O↓+2H2O;
;CH2=C(CH3)-CHO+2Cu(OH)2$\stackrel{△}{→}$CH2=C(CH3)-COOH+Cu2O↓+2H2O; ;
;
(3)H为CH2=C(CH3)-COOH,与H具有相同官能团的H的同分异构体有CH2=CHCH2COOH 和CH3CH=CHCOOH,故答案为:CH2=CHCH2COOH 和CH3CH=CHCOOH.
点评 本题考查有机物的推断,解答关键是找解题的突破口,根据A→B+C(水解反应)可以判断A、B、C分别是酯、羧酸和醇,且由(1)可以确定B和C的结构,以此可推断其它物质,注意有机物官能团的结构和性质,为正确解答该类题目的关键,题目难度中等.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 大于2cmol/L | B. | 小于2cmol/L | ||
| C. | 等于2cmol/L | D. | 在cmol/L和2cmol/L之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 )的废水可以利用微生物电池除去,其原理如图2所示.
)的废水可以利用微生物电池除去,其原理如图2所示. +2e-+H+═
+2e-+H+═ +Cl-.
+Cl-.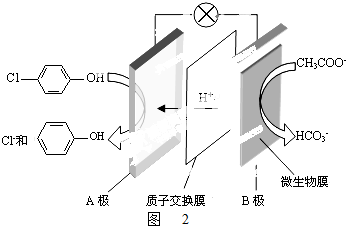
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀HNO3溶液溶解FeS固体:FeS+2H+═Fe2++H2S | |
| B. | Fe2(SO4)3的酸性溶液中通过足量硫化氢:2Fe3++H2S═2Fe2++S↓+2H+ | |
| C. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3+2HClO | |
| D. | 酸性条件下KIO3溶液与KI溶液反应生成I2:IO3-+5I-+3H2O═3I2+6OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 非金属性 | B. | 氢化物的稳定性 | ||
| C. | 单质熔点 | D. | 最高价氧化物对应水化物酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氯化钠固体不导电,所以氯化钠是非电解质 | |
| B. | 向纯水中加入碳酸钠能使水的电离平衡正向移动,水的离子积增大 | |
| C. | 如右图研究的是铁的吸氧腐蚀,实验中红色首先在食盐水滴的中心出现 | |
| D. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s) 的△H<0△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验要求 | 答案 | 供选择的化学试剂及方法 |
| a | 检验乙酸是否具有酸性 | A.新制的氢氧化铜悬浊液 | |
| b | 检验植物油中是否含有碳碳双键 | B.紫色石蕊试液 | |
| c | 检验尿液中是否含有葡萄糖 | C.加入饱和Na2CO3溶液,分液 | |
| d | 除去乙酸乙酯中的少量乙酸 | D.溴水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com