
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4 L CCl4中含CCl4分子数为NA
B. 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等
C. 0.1 mo1·L-1 MgCl2溶液中含Cl-数为0.2NA
D. 3.9 g Na2O2 晶体中含有的离子总数为0.2NA
【答案】B
【解析】
A、标况下四氯化碳为液态;B、依据n=![]() 计算物质的量,结合铁和氯气反应生成氯化铁,铜和氯气反应生成氯化铜,等物质的量反应需要判断过量问题;C、氯化镁溶液的体积不知,无法计算氯化镁的物质的量;D.n(Na2O2)=
计算物质的量,结合铁和氯气反应生成氯化铁,铜和氯气反应生成氯化铜,等物质的量反应需要判断过量问题;C、氯化镁溶液的体积不知,无法计算氯化镁的物质的量;D.n(Na2O2)=![]() =0.05mol,Na2O2晶体中含有钠离子和过氧根离子。
=0.05mol,Na2O2晶体中含有钠离子和过氧根离子。
A、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和共价键数目,选项A错误;B、5.6g铁物质的量=![]() =0.1mol,6.4g铜物质的量=
=0.1mol,6.4g铜物质的量=![]() =0.1mol,分别与0.1mol氯气完全反应,铜恰好反应,铁过量,所以反应过程中转移的电子数相等,选项B正确;C、题中没有告诉氯化镁溶液的体积,无法计算氯化镁的物质的量及氯离子数目,选项C错误;B.Na2O2晶体中含有钠离子和过氧根离子,n(Na2O2)=
=0.1mol,分别与0.1mol氯气完全反应,铜恰好反应,铁过量,所以反应过程中转移的电子数相等,选项B正确;C、题中没有告诉氯化镁溶液的体积,无法计算氯化镁的物质的量及氯离子数目,选项C错误;B.Na2O2晶体中含有钠离子和过氧根离子,n(Na2O2)=![]() =0.05mol,含有的离子总数为0.15NA,选项D错误;答案选B。
=0.05mol,含有的离子总数为0.15NA,选项D错误;答案选B。


科目:高中化学 来源: 题型:
【题目】下列说法或表示法正确的是
A. 氢气与氧气反应生成等量的水蒸气和液态水,前者放出热量多
B. 需要加热的反应说明它是吸热反应
C. 在稀溶液中:H+(aq)+OH-(aq) =H2O(l) ΔH=-57.3 kj/mol,若将含0.5 mol H2SO4 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D. 由N2O4(g) ![]() 2NO2(g) △H=-56.9 kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ
2NO2(g) △H=-56.9 kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物H可用于光刻工艺中,作抗腐蚀涂层。下面是高聚物H的合成路线:
![]()

Ⅱ.反应③属于加聚反应 Ⅲ.D属于高分子化合物,
请回答下列问题:
(1)反应⑤的条件是_______________;E的分子式为__________________;
(2)C中含有的官能团的名称是________________ ;
(3)芳香烃M与A的实验式相同,经测定M的核磁共振氢谱有5组峰且峰面积比为1:1:2:2:2,则M的结构简式为_____________ ;推测M可能发生的反应类型是___________;(写出一种即可)
(4)反应⑦的化学方程式为___________________________________________________ ;
(5)D和G反应生成H的化学方程式为___________________________________________ ;
(6)G的同分异构体中,与G具有相同官能团的芳香族化合物还有__________种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成都需要用它。
(1)工业上通常采用电解法制氯气,请观察图后回答下列问题:

① 请写出该反应的化学方程式________________________________。
② 通电后,b侧产生的气体是______![]() 填化学式
填化学式![]() 。
。
(2)某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉![]() 这是一个放热反应
这是一个放热反应![]() ,回答下列问题:
,回答下列问题:

①在A装置中用固体二氧化锰与浓盐酸,在加热条件下制取氯气,请写出反应的化学方程式________________________________。
②漂白粉将在U形管中产生,其化学方程式是______________________________。
③装置C的作用是______________。
④此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
I.温度较高时氯气与消石灰反应生成![]() ,为避免此副反应的发生,可采取的措施是________________________。
,为避免此副反应的发生,可采取的措施是________________________。
II.试判断另一个副反应![]() 用化学方程式表示
用化学方程式表示![]() ______________________________,为避免此副反应的发生,可以在A与B之间连接一个装有______的洗气瓶。
______________________________,为避免此副反应的发生,可以在A与B之间连接一个装有______的洗气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
A. 反应中硫酸作氧化剂
B. ![]() 中硫元素被氧化
中硫元素被氧化
C. 刺激性气味的气体是氨气
D. 1mol![]() 完全反应转移0.5mol电子
完全反应转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态铜原子的电子排布式为______;价电子中成对电子数有____个。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是_________。
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3___H3PO4(填“>”或“<”),从结构的角度说明理由:__________________________。
(3)磷青铜中的锡、磷两元素电负性的大小为Sn___P(填“>”“<”或“=”)。
(4)某磷青铜晶胞结构如图所示。
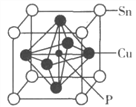
①则其化学式为________。
②该晶体中距离Cu原子最近的Sn原子有______个,这些Sn原子所呈现的构型为_________。
③若晶体密度为8.82g·cm-3,最近的Cu原子核间距为____pm(用含NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是 ( )
A | B | C | D | |
反应 装置或 图像 |
|
|
|
|
实验现 象或图 像信息 | 温度计的 水银柱不 断上升 | 反应物总能 量大于生成 物总能量 | 反应开始后, 甲处液面低 于乙处液面 | 反应开始 后,针筒活 塞向右移动 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com