
����Ŀ��ʵ�������ܶ�Ϊ1.25 g mL-1����������Ϊ36.5%��Ũ��������240 mL 0.1 mol L-1�����ᣬ��ش��������⣺
��1��Ũ��������ʵ���Ũ��Ϊ ��
��2������ 240 mL 0.1 mol L-1������
Ӧ��ȡŨ�������/mL | Ӧѡ������ƿ�Ĺ��/mL |
��1������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ� ��
A����30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ����
B������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL��, �ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע������ƿ��
D��������ƿ�ǽ�����ҡ��
E.���ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�������
F.����������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm��
��4����ʵ�������������������������Һ�����ʵ���Ũ���к�Ӱ�죨����ƫ��������ƫ������������������
������ϡ��������ձ�δϴ�ӣ� ��
������ƿ��ԭ����������ˮ�� ��
������ʱ�۲�Һ�温�ӣ� ��
��5����ʵ������г������������δ�����
������ʱ������ˮʱ�����˿̶� ��
��������ƿ��ת����Һʱ�й�Һ��������Һ���� ��
������ҡ�����Һ���½� ��
���𰸡���1��12.5mol/L����2��2.0��250����3��BCAFED��
��4����ƫ�ͣ������䣬��ƫ�ߣ�
��5�����������ƣ����������ƣ����������䡣
�������������������1��ʵ�������ܶ�Ϊ1.25 g mL-1����������Ϊ36.5%��Ũ��������240 mL 0.1 mol L-1�����ᣬ����ʵ����û��240mL������ƿ�������Ҫ����250mL��Һ��������HCl�����ʵ���Ϊ��n��HCl��=0.25L��0.1 mol L-1=0.025mol������HCl������Ϊ��m��HCl��=0.025mol��36.5g mol-1=0.9125g����Һ������Ϊ��![]() ������Һ�����
������Һ�����![]() ��������ʵ����ʵ���Ũ��Ϊ��
��������ʵ����ʵ���Ũ��Ϊ�� ����2��������������֪��Ӧ��ȡŨ��������Ϊ2.0mL����Ҫѡ������ƿ�Ĺ����250mL����ƿ����3��������Һʱ����һ��������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL��, �ò���������������ʹ���Ͼ��ȣ��ڶ�����������ȴ�������ز�����ע������ƿ�У�����������30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ�������IJ�������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm�������岽�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶������У���������.������ƿ�ǽ�����ҡ�ȣ����װƿ���档��������Һ����ȷ˳����BCAFED ����4�����ݹ�ʽ��c=n/V������������������ϡ��������ձ�δϴ�ӣ�ʹ���ʵ����ʵ���ƫС����Һ������䣬�����Һ�����ʵ���Ũ��ƫ�ͣ�������ƿ��ԭ����������ˮ������Һ�����ƹ�����Ӱ�죬�����ʵ����ʵ���Ũ�Ȳ��䣻������ʱ�۲�Һ�温�ӣ���Һ�����ƫС��������ʵ����ʵ���Ũ��ƫ�ߡ���5��������ʱ������ˮʱ�����˿̶ȣ���������������Һ����������ƿ��ת����Һʱ�й�Һ��������Һ���������ʵ����ʵ���ƫС������������Һ�����ʵ���Ũ�Ȳ��������������ƣ�������ҡ�����Һ���½��������������ơ�
����2��������������֪��Ӧ��ȡŨ��������Ϊ2.0mL����Ҫѡ������ƿ�Ĺ����250mL����ƿ����3��������Һʱ����һ��������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL��, �ò���������������ʹ���Ͼ��ȣ��ڶ�����������ȴ�������ز�����ע������ƿ�У�����������30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ�������IJ�������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm�������岽�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶������У���������.������ƿ�ǽ�����ҡ�ȣ����װƿ���档��������Һ����ȷ˳����BCAFED ����4�����ݹ�ʽ��c=n/V������������������ϡ��������ձ�δϴ�ӣ�ʹ���ʵ����ʵ���ƫС����Һ������䣬�����Һ�����ʵ���Ũ��ƫ�ͣ�������ƿ��ԭ����������ˮ������Һ�����ƹ�����Ӱ�죬�����ʵ����ʵ���Ũ�Ȳ��䣻������ʱ�۲�Һ�温�ӣ���Һ�����ƫС��������ʵ����ʵ���Ũ��ƫ�ߡ���5��������ʱ������ˮʱ�����˿̶ȣ���������������Һ����������ƿ��ת����Һʱ�й�Һ��������Һ���������ʵ����ʵ���ƫС������������Һ�����ʵ���Ũ�Ȳ��������������ƣ�������ҡ�����Һ���½��������������ơ�


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڳ�����������һ����( )
A. Cl2��O2��FeCl3��KMnO4
B. O2��KMnO4��C��H2
C. Na��K��FeCl2��H2��CO
D. CuO��CO��Fe2O3��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1mol̼����������ȫȼ���������壬�ų�393kJ�������������Ȼ�ѧ����ʽ��ʾ��ȷ����
A. C(s)+O2(g)��CO2(g)+393kJ
B. C + O2�� CO2+393kJ
C. C (s) + O2 (g)��CO2 (g)-393kJ
D. C (s) +1/2O2 (g) �� CO(g) +393kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ������������ѧ��Ӧ���п����̶ȵ���������������ijͬѧ�ⶨ��ѧ��Ӧ���ʲ�̽����Ӱ�����ص�ʵ�顣
��.�ⶨ��ѧ��Ӧ����
��ͬѧ������ͼװ�òⶨ��ѧ��Ӧ���ʡ�(��֪��S2O32-��2H�� = H2O��S����SO2��)

(1) Ϊ��֤ʵ��ȷ�ԡ��ɿ��ԣ����ø�װ�ý���ʵ��ǰӦ�Ƚ��еIJ����� ������ͼ��ʾ��ʵ����Ʒ�������⣬����Ҫ��һ��ʵ��������______ ��
(2)����2 minʱ�ռ���224 mL(������ɱ�״��)���壬�ɼ������2 min��H���ķ�Ӧ���ʣ����òⶨֵ��ʵ��ֵƫС����ԭ���� ��
(3)�Լ����ⶨ�÷�Ӧ�Ļ�ѧ��Ӧ���ʵ���������(дһ��)��
��.Ϊ̽�ֻ�ѧ��Ӧ���ʵ�Ӱ�����أ���Ƶ�ʵ�鷽�����±���
(��֪ I2��2S2O32- = S4O62-��2I��������Na2S2O3��Һ������)
ʵ����� | ���V/mL | ʱ��/s | |||
Na2S2O3��Һ | ������Һ | ��ˮ | ˮ | ||
�� | 10.0 | 2.0[ | 4.0 | 0.0 | t1 |
�� | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
�� | 6.0 | 2.0 | 4.0 | Vx | t3 |
(4)��ʵ����е�Ŀ���� ������Vx�� mL���Ƚ�t1��t2��t3��С�����Ʋ��ʵ����ۣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����O2��C��CO��CuO��NaHCO3��ϡ������������������ϣ���CO2���ɵĻ�ѧ��Ӧ��( )
A��3�� B��4�� C��5�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£��赥�ʺ�HCl��Ӧ����SiHCl3�Ǵֹ��ᴿ����Ҫ���衣ijС�������ͼ��ʾװ���������ת�����г�װ����ȥ����
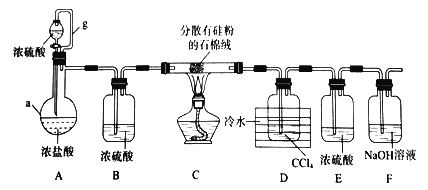
��֪��SiHCl3�ķе�Ϊ33.0��C���������л��ܼ�������ˮ���ҷ�Ӧ���ڿ������ױ�������CCl4�ķе�Ϊ76.8��C����ش�
��1������a������Ϊ ������g������Ϊ ��
��2��װ��A�У�Ũ�������ֵ�����Ϊ ��ʵ��ʱ�����ȴ�Һ©��������һ��ʱ����ڵ�ȼC���ƾ��ƣ������� ��
��3��װ��C�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��4��װ��D�����õ�Һ̬�����ķ��뷽��Ϊ ���������������
��5����Ӧ�������ͨ��װ��F�е�NaOH��Һ���ݳ�����Ĵ�������Ϊ ��
��6��SiHCl3�ڳ�ʪ�Ŀ����б�����������һ���������һ�������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������˵����ȷ������ ��
A����״���£�22.4 L��CCl4��C��Cl����ΪΪ4NA
B�������£�1 L 0.1molL��1��![]() ��Һ�е�ԭ����Ϊ0.2 NA
��Һ�е�ԭ����Ϊ0.2 NA
C���ڷ�ӦKIO3+6HI��KI+3I2+3H2O�У�ÿ����3molI2ת�Ƶĵ�����Ϊ6 NA
D��0.1mol������0.1mol�Ҵ���Ӧ�������������ķ�����Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ����������
A. ![]() ����Һ�У�Na+��K+��SiO32����SO32-
����Һ�У�Na+��K+��SiO32����SO32-
B. pH��1����Һ�У�K+��Al3+��SO42-��F��
C. ��þ��Ӧ������������Һ�У�Na+��Ba2+��NO3-��Cl-
D. 0��1mol/L��NaHCO3��Һ�У�NH4+��Mg2+��Br-��AlO2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʯ��ʯī��Ϊ̼��ͬ�������壬����ȼ��ʱ����������������һ����̼�������ȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ��
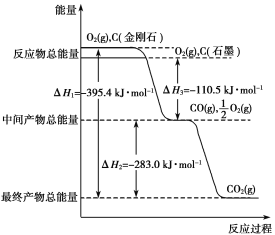
(1)�������Ľ��ʯ��ʯī��ȫȼ�գ�____________(�������ʯ������ʯī��)�ų����������࣬д����ʾʯīȼ���ȵ��Ȼ�ѧ����ʽ��_______________________��ע�⣺ʯī����C(ʯī��s)����ʾ��
(2)��ͨ��״���£�____________(�������ʯ������ʯī��)���ȶ���
(3)6 gʯī��һ����������ȼ�գ���������18 g���ù����зų�������Ϊ______________kJ��
�������ס�������������ͬ�������壬�ڿ�����ȼ�յõ����������������ʱ����P4O6����������ʱ����P4O10��
(1)��֪298 Kʱ���ס�������ȫȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ��
P4(���ף�s)��5O2(g)=P4O10(s) ��H1����2 983.2 kJ��mol��1
4P(���ף�s)��5O2(g)= 4 P4O10(s) ��H2����2954 kJ��mol��1
����¶��°���ת��Ϊ�����Ȼ�ѧ����ʽ��4P(���ף�s) ==P4(���ף�s)��H��____________
(2)��֪298 Kʱ���ײ���ȫȼ�յ��Ȼ�ѧ����ʽΪ��P4(���ף�s)��3O2(g)=P4O6(s) ��H����1 638 kJ��mol��1����ij�ܱ������м���62 g����50.4 L����(��״��)����������ʹ֮ǡ����ȫ��Ӧ�������õ���P4O10��P4O6�����ʵ���֮��Ϊ_________________����Ӧ�����зų�������Ϊ___________kJ��
(3)��֪����PCl3�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ���(kJ��mol��1)��
P��P��198��Cl��Cl ��243��P��Cl��331��
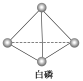
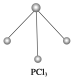
��ӦP4(���ף�s)��6Cl2(g)=4PCl3(s)�ķ�Ӧ����H��_______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com