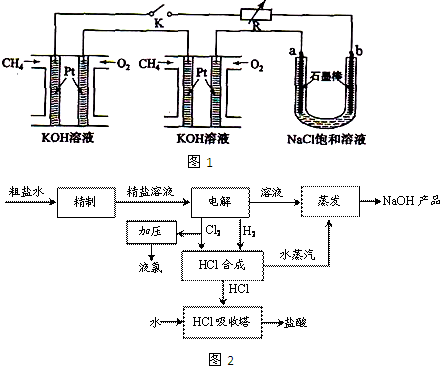
(2012?长宁区一模)Ⅰ.工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅.
(1)原料粗盐中常含有泥沙和Ca
2+、Mg
2+、Fe
3+、SO
42-等杂质,必须精制后才能供电解使用.精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na
2CO
3、②HCl(盐酸)③BaCl
2,这3种试剂添加的合理顺序是
③①②
③①②
(填序号)洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
③
③
.(填序号)(①饱和Na
2CO
3溶液 ②饱和K
2CO
3溶液 ③75%乙醇 ④四氯化碳)
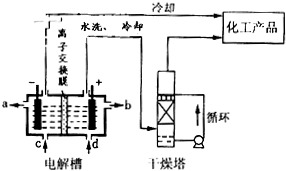
(2)如图是离子交换膜(允许钠离子通过,不允许氢氧根与氯离子通过)法电解饱和食盐水示意图,电解槽阳极产生的气体是
氯气
氯气
;NaOH溶液的出口为
a
a
(填字母);精制饱和食盐水的进口为
d
d
(填字母);干燥塔中应使用的液体是
浓硫酸
浓硫酸
.
Ⅱ.多晶硅主要采用SiHCl
3还原工艺生产,其副产物SiCl
4的综合利用受到广泛关注.
(1)SiCl
4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl
4与H
2和O
2反应,产物有两种,化学方程式为
.
(2)SiCl
4可转化为SiHCl
3而循环使用.一定条件下,在20L恒容密闭容器中的反应:
3SiCl
4(g)+2H
2(g)+Si(s)?4SiHCl
3(g)
达平衡后,H
2与SiHCl
3物质的量浓度分别为0.140mol/L和0.020mol/L,若H
2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为
0.351
0.351
kg.
(3)实验室制备H
2和Cl
2通常采用下列反应:
Zn+H
2SO
4→ZnSO
4+H
2↑;MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
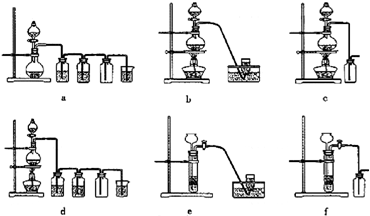
据此,从下列所给仪器装置中选择制备并收集H
2的装置
e
e
(填代号)和制备并收集干燥、纯净Cl
2的装置
d
d
(填代号).
可选用制备气体的装置:
(4)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气
134.4
134.4
m
3(标准状况).(忽略可能存在的其他反应)
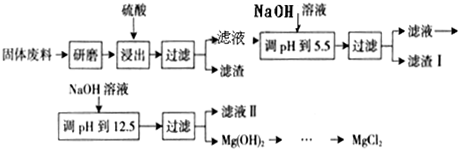
某工厂生产硼砂过程中产生的固体废料,主要含有MgCO
3、MgSiO
3、CaMg(CO
3)
2、Al
2O
3和Fe
2O
3等,回收其中镁的工艺流程如下:
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
| PH |
3.2 |
5.2 |
12.4 |
Ⅲ.部分阳离子以氢氧化物形式完全沉淀时溶液的pH见上表,请回答下列问题:
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
适当提高反应温度、增加浸出时间
适当提高反应温度、增加浸出时间
(要求写出两条).
(2)滤渣I的主要成分是
Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
.
Mg(ClO
3)
2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl
2+2NaClO
3→Mg(ClO
3)
2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如图所示:
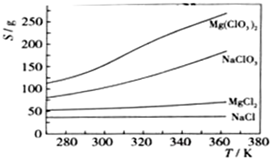
(3)将反应物按化学反应方程式计量数比混合制备Mg(ClO
3)
2.简述可制备Mg(ClO
3)
2的原因:
在某一温度时,NaCl最先达到饱和析出;Mg(ClO3)2的溶解度随温度变化的最大,NaCl的溶解度与其他物质的溶解度有一定的差别;
在某一温度时,NaCl最先达到饱和析出;Mg(ClO3)2的溶解度随温度变化的最大,NaCl的溶解度与其他物质的溶解度有一定的差别;
.
(4)按题(3)中条件进行制备实验.在冷却降温析出Mg(ClO
3)
2过程中,常伴有NaCl析出,原因是:
降温前,溶液中NaCl已达饱和,降低过程中,NaCl溶解度会降低,会少量析出;
降温前,溶液中NaCl已达饱和,降低过程中,NaCl溶解度会降低,会少量析出;
.除去产品中该杂质的方法是:
重结晶
重结晶
.

 阅读快车系列答案
阅读快车系列答案

 (2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究: