
| A. | 三个烧杯中均会发生的离子反应为2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 三个烧杯中钠均在液面上剧烈反应,且X烧杯中反应最剧烈 | |
| C. | 三个烧杯反应后,生成的溶质的物质的量浓度相同 | |
| D. | 三个烧杯反应后,生成的气体的质量一定相同 |
分析 钠密度小于水,钠投入溶液中,发生的反应实质是钠与酸或者水电离产生的氢离子的反应,溶液中氢离子浓度越大,反应越剧烈,生成的氢氧化钠又能够与硫酸铜发生复分解反应,据此解答.
解答 解:A.钠投入溶液中,发生的反应实质是钠与酸或者水电离产生的氢离子的反应,钠与盐酸反应的实质为:2Na+2H+=2Na++H2↑,故A错误;
B.盐酸为酸、硫酸铜为强酸弱碱盐水解显酸性,所以X、Y、Z三种溶液中,氢离子浓度由大到小的顺序为:Y Z X,氢离子浓度越大,反应越剧烈,水中氢离子浓度最小,所以反应最缓和,故B错误;
C.100mL水、100mL 0.1mol•L-1盐酸、100mL 0.01mol•L-1硫酸铜溶液的X、Y、Z三个烧杯中各投入0.05mol Na,分别生成0.05mol 氢氧化钠,0.01mol的氯化钠和0.04mol的氢氧化钠、硫酸铜溶液反应,方程式为:2Na+2H2O=2NaOH+H2↑,2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,生成0.025mol的硫酸钠,所以Z烧杯中溶质的浓度最小,故C错误;
D.依据得失电子守恒,可知相同量的钠失去电子数相同,生成氢气的量相同,故D正确;
故选:D.
点评 本题考查了钠的性质,解题关键在于明确钠与溶液反应的实质,题目难度不大,注意知识的积累.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
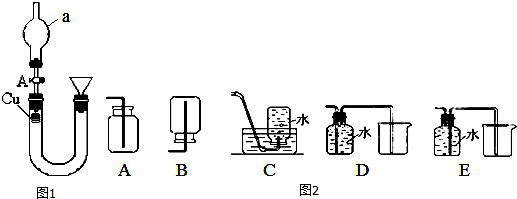
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C14H16O4 | B. | C14H18O5 | C. | C16H22O5 | D. | C16H20O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池为一次电池 | |
| B. | 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═Mn2O3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 化学反应中能量变化的主要原因是物质状态的改变 | |
| B. | 铝与盐酸的反应中,反应物的总能量比生成物的总能量高 | |
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图II所示的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验剩余的药品不能放回原试剂瓶 | |
| B. | 点燃可燃性气体前必须验纯 | |
| C. | 气体实验装置在实验前要进行气密性检查 | |
| D. | 滴管不能交叉使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com