
【题目】过量铝粉分别与下列4种等体积的溶液充分反应,放出氢气最多的是( )
A.3mol·L-1H2SO4溶液B.18mol·L-1H2SO4溶液
C.1.5 mol·L-1KOH溶液D.3mol·L-1HNO3溶液
【答案】A
【解析】
设各溶液的体积为VL,根据化学反应的事实及关系式的定量计算分析判断。
A. 铝粉与H2SO4溶液反应的化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑,3H2SO4![]() 3H2,则3mol·L-1H2SO4溶液生成氢气的物质的量为3V mol,
3H2,则3mol·L-1H2SO4溶液生成氢气的物质的量为3V mol,
B. 18mol·L-1H2SO4溶液为浓硫酸,常温下,铝遇到浓硫酸会发生钝化,没有氢气放出,B项不选;
C. 铝粉与1.5 mol·L-1KOH溶液反应的化学方程式为:2Al+2KOH+2H2O=2KAlO2+3H2↑,2KOH![]() 3H2,则生成氢气的物质的量为1.5V
3H2,则生成氢气的物质的量为1.5V![]() =2.25V mol;
=2.25V mol;
D. 3mol·L-1HNO3溶液为稀硝酸,铝粉与3mol·L-1HNO3溶液在常温下发生氧化还原反应生成一氧化氮,没有氢气放出,D项不选;
根据上述分析可知,因3V >2.25V,即过量铝粉与3mol·L-1H2SO4溶液反应比与1.5 mol·L-1KOH溶液反应放出的氢气最多,A项正确,
答案选A。


科目:高中化学 来源: 题型:
【题目】氯化亚锡用途广泛,在无机工业中用作还原剂,在口腔护理行业中,二水氯化亚锡多用于防龋齿脱敏类牙膏中,以预防龋齿的发生。某研究小组制取二水氯化亚锡工艺流程如下:
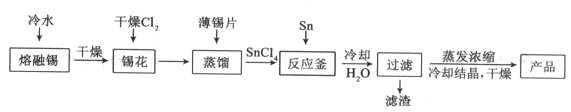
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。
(1)四氯化锡暴露于空气中与空气中水分反应生成白烟,有强烈的刺激性气味,生成偏锡酸(H2SnO3),写出该反应的化学方程式______;
(2)将金属锡熔融,然后泼入冷水,激成锡花,其目的是______;
(3)在制备二水氯化亚锡时,温度对锡转化率的影响如图1所示,则该反应应控制的温度范围为______℃;
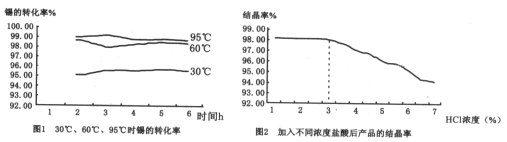
(4)反应原料中盐酸浓度对结晶率的影响如图2所示,则盐酸浓度应控制的范围为______,原因______。
(5)反应釜中发生反应的化学方程式为______;
(6)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应)
①将该试样溶于盐酸,发生反应为Sn+2HCl=SnCl2+H2↑;
②加入过量FeCl3溶液
③用已知浓度的K2Cr2O7滴定②中生成的Fe2+,则反应的离子方程式为______;
(7)取1.125g锡粉,经上述各步反应后,共用去0.1000mol/LK2Cr2O7溶液 30.00mL,锡粉中锡的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图的装置进行电解实验:A极是铜锌合金,B为纯铜。电解质溶液中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,此时B极质量增加9.6g,溶液质量增加0.05g,则A极合金中Cu、Zn原子个数比为

A. 4:1 B. 1:1 C. 2:1 D. 任意比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
丹参素是中药丹参的水溶性成分,结构为 F ,具有扩张血管、增加冠脉血流量等作用,某一种合成路线如下图所示:
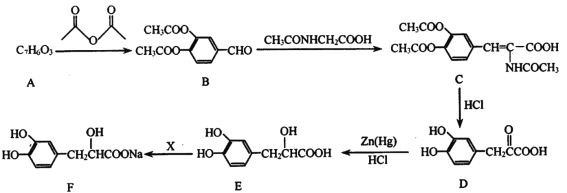
已知:![]()
![]()
(1)丹参素的分子式为____________; D →E 的反应类型是_______________。
(2)试剂X是____________(写化学式);C 中含氧官能团名称为_____________。
(3) A→B 的反应方程式为________________。
(4)G与 E互为同分异构体,请写出满足下列条件的任意两种G的结构简式______________。
①lmolG 能与4molNaOH发生反应;
②能够发生水解反应;
③核磁共振氢谱显示5个吸收峰,且峰面积之比为 1 : 2 : 2 : 2 : 3 。
(5)参考上述流程信息,设计以![]() 、CH3CHO为原制取
、CH3CHO为原制取![]() 的合成路线(其它无机试剂任选)。________________
的合成路线(其它无机试剂任选)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将AgNO3溶液分别滴加到浓度均为0.01mol/L的NaBr、Na2SeO3溶液中,所得的沉淀溶解平衡曲线如图所示(Br-、SeO32-用Xn-表示,不考虑SeO32-的水解)。下列叙述正确的是
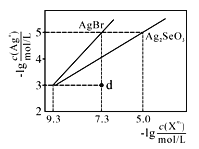
A. Ksp(Ag2SeO3)的数量级为10-10
B. d点对应的AgBr溶液为不饱和溶液
C. 所用AgNO3溶液的浓度为10-3 mol/L
D. Ag2SeO3(s)+2Br-(aq)==2AgBr(s)+SeO32- (aq)平衡常数为109.6,反应趋于完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
![]() ―→
―→![]()
某化学兴趣小组将上述流程②③设计成如图所示:
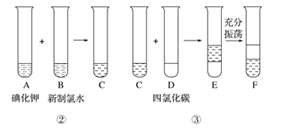
已知②中发生反应的化学方程式为Cl2+2KI=2KCl+I2
回答下列问题:
(1)写出提取过程①③中实验操作名称:①____,③____。
(2)四氯化碳是____色、密度比水____的液体。Y中下层液体的颜色为___色,上层液体中溶质的主要成分为_____。
(3)从碘的四氯化碳溶液中得到碘需进行的操作是______。
(4)在操作①过程中,使用到的实验仪器有____(多选)。
A.试管 B.烧杯 C.玻璃棒 D.蒸发皿 E.漏斗 F.铁架台 G.分液漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有铁的氧化物样品,用150 mL 5 mol/L的盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下氯气1.68L,使其中的Fe2+全部转化为Fe3+,该样品可能的化学式是( )
A.Fe2O3B.Fe3O4C.Fe5O7D.Fe4O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表的说法正确的是( )
A. 元素周期表有7个周期,8个主族
B. 元素周期表有18个纵行,共16个族
C. 短周期元素中可能有副族元素
D. 在元素周期表中的金属元素和非金属元素交界处最容易找到优良的催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com