
| A. | ①②④⑥ | B. | ①③ | C. | ②④⑤⑥ | D. | ③⑤ |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性键、同种非金属元素之间易形成非极性键,含有离子键的化合物为离子化合物,只含共价键的化合物为共价化合物.
解答 解:①硅晶体只只含有非极性键,属于原子晶体,故错误;
②H2O2分子中H原子和O原子之间为极性键、O原子和O原子之间只存在非极性键,属于共价化合物,故错误;
③CaC2中钙离子和C22-之间存在离子键、C原子与C原子之间存在非极性键,属于离子化合物,故正确;
④NH4Cl中铵根离子与氯离子之间存在离子键,N与H之间形成共价键,属于离子化合物,故错误;
⑤Na2O2中钠离子和过氧根离子之间存在离子键、O原子之间存在非极性键,属于离子化合物,故正确;
⑥苯酚中C与C之间存在非极性键,C与O之间存在极性键,属于共价化合物,故错误.
故选D.
点评 本题考查离子键、极性键和非极性键,侧重考查基本概念,明确概念的内涵即可解答,会正确书写过氧化钠电子式,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
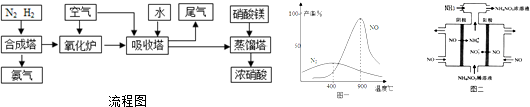
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | 若反应物所具有的总能量小于生成物所具有的总能量,则发生的是放热反应 | |
| C. | 稀H2SO4溶液与稀Ba(OH)2溶液反应生成lmol H2O时放出的热量叫中和热 | |
| D. | 1molH2与0.5molO2反应放出的热量就是H2的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-=AlO2-+2H2O | |
| B. | 向NaOH溶液中通入少量的CO2:OH-+CO2=HCO3- | |
| C. | 向Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
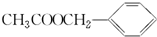 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: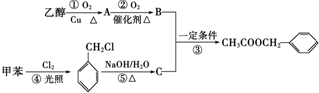
 .
.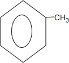 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl.
+HCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol•L-1CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 向0.1mol•L-1CH3COONa溶液加入少量水,溶液中$\frac{c(CHCO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 | |
| C. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(C{l}^{-})}$>1 | |
| D. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中$\frac{c(Cl-)}{c(B{r}^{-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、D2、T2互为同素异形体 | B. | 甲烷和异丁烷互为同系物 | ||
| C. | 14C和C60互为同位素 | D. | 淀粉和纤维素互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com