
【题目】某温度下,在2L密闭容器中充入4molA气体和3molB气体,发生下列反应:2A(g)+B(g) ![]() C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。
C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。
(1)求x =____。
(2)求这段时间A的平均反应速率为_____。
(3)平衡时B的浓度为______。
(4)求该温度下反应平衡常数为_____________
科目:高中化学 来源: 题型:
【题目】传统接触法制取硫酸能耗大,污染严重。将燃料电池引入 硫酸生产工艺可有效解决能耗和环境污染问题,同时提供电能 以燃料电池为电源电解硫酸铜溶液的工作原理示意图如下所示。下列说法不正确的是( )

A.若 a 极消耗 2.24LSO2,理论上 c 极有 6.4g 铜析出
B.H+由 a 极通过质子交换膜向 b 极移动
C.该燃料电池的总反应式为 2SO2+O2+2H2O=2H2SO4
D.b 极为正极,电极反应式为 O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华文化源远流长,如![]() 本草图经
本草图经![]() 中曾有对青矾的描述:“形似朴硝
中曾有对青矾的描述:“形似朴硝![]() 而绿色,取此物置于铁板上,聚碳,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金升者是真也。”对于文中描述,下列说法正确的是
而绿色,取此物置于铁板上,聚碳,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金升者是真也。”对于文中描述,下列说法正确的是![]()
![]()
A.朴硝既不属于电解质也不属于非电解质
B.青矾的成分为![]()
C.文中使用了蒸发结晶的分离方法
D.文中的反应涉及了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 实验室中常用排饱和食盐水的方法收集Cl2
B. 对CO(g)+NO2(g)![]() CO2(g)+NO(g),平衡体系增大压强可使颜色变深
CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C. 升高温度能够促进水的电离
D. 在含有Fe(SCN)3的红色溶液中加少量铁粉,振荡静置,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2H2(g)+O2(g) ![]() 2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g)
2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq)
2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq) ![]() H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
A. CH3OH的燃烧热为1452 kJ·mol-1
B. 2H2(g)+O2(g) ![]() 2H2O(g) H > -571.6 kJ·mol-1
2H2O(g) H > -571.6 kJ·mol-1
C. CH3COOH(aq)+NaOH(aq) ![]() H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
D. 2CH3OH(l)+O2(g) ![]() 2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,有关化学反应和能量变化的说法不正确的是
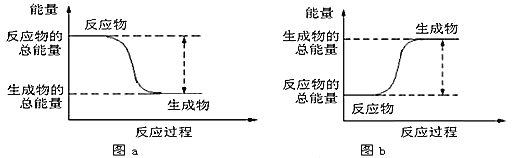
A. 图a表示的是放热反应的能量变化
B. 图b表示反应物的键能总和高于生成物的键能总和
C. 图b 可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
D. 图a不需要加热就一定能发生,图b一定需要加热才能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是![]()
A.工业制普通玻璃、工业炼铁的原料都需用到石灰石
B.接触法制硫酸工业中,![]() 转变为
转变为![]() 的反应在热交换器中进行
的反应在热交换器中进行
C.生物炼铜法是细菌利用氧气将硫化铜转化为硫酸铜,使铜的冶炼变得十分简单
D.电解饱和食盐水可制取氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中两种元素组成。常温下,甲是一种含氮质量分数为87.5%的液态化合物,相对分子质量与空气中某种主要成份的相对分子质量相同;乙和丙是铜的两种常见氧化物,乙是新制的氢氧化铜与乙醛反应的还原产物。试回答下列问题:
(1)甲的结构式___。
(2)甲和丙反应的产物中含有乙和一种气态单质,写出其化学方程式___。
(3)向乙固体中加入过量硫酸酸化的硫酸铁溶液,乙固体完全溶解,得到透明溶液。
①写出其离子方程式___。
②若所得溶液阳离子浓度均约为0.1molL-1,再向所得混合液中加丙,最先得到___沉淀(不同浓度的金属离子开始和完全以氢氧化物沉淀的pH如图)。

③向上述混合液加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相)R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。试设计实验验证有机相中含有铜元素___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com