
分析 发生反应:2H2+O2═2H2O,计算2mol氢气反应放出的热量,焓变△H<0,注明物质聚集状态与反应热,书写热化学方程式.
解答 解:标况下,5.6L氢气物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,则2mol氢气反应放出的热量为:71.45kJ×$\frac{2mol}{0.25mol}$=571.6kJ,故热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,
故答案为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol.
点评 本题考查了热化学方程式的书写方法,注意物质状态和焓变的计算,题目较简单.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性强弱顺序是:Fe3+>Cl2>I2>SO42- | |
| B. | 还原性强弱顺序是:SO2>I->Fe2+>Cl- | |
| C. | 反应Cl2+SO2+2H2O═2HCl+H2SO4不能发生 | |
| D. | Fe3+与I-在溶液可以大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰融化时,分子中氢氧键发生断裂 | |
| B. | 原子晶体中共价键越强,熔点和沸点越高 | |
| C. | 分子晶体中共价键键能越大,该分子晶体的熔点和沸点一定也越高 | |
| D. | 分子晶体中分子间作用力越大,该物质越稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取5.26ml盐酸 | |
| B. | 用托盘天平称取11.70g食盐 | |
| C. | 用PH试纸测得溶液的PH是3.5 | |
| D. | 用标准NaOH溶液滴定未知浓度的盐酸用去23.10ml NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: |
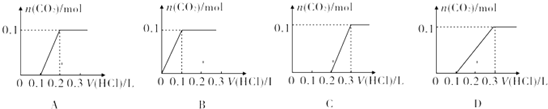
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com