
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量水能使溶液恢复到电解前的浓度的是( )
A.AgNO3 B.Na2SO4
C.CuCl2 D.HCl
科目:高中化学 来源: 题型:
如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
A.A、B简单离子半径大小关系为B3+>A2+
B.D、E形成的简单离子的还原性:E->D-
C.气态氢化物的稳定性:HD<H2C
D.最高价氧化物对应的水化物的酸性:H2CO4>HEO4
查看答案和解析>>
科目:高中化学 来源: 题型:
G是一种合成橡胶和树脂的重要原料,A是C、H、O三种元素组成的五元环状化合物,相对分子质量为98,其核磁共振氢谱只有一个峰;F的核磁共振氢谱有3个峰,峰面积之比为2:2:3。已知:(其中R是烃基)

有关物质的转化关系如下图所示,请回答以下问题。

(1)A中不含氧的官能团的名称是 ;⑤的反应类型是 。G的结构简式为 ;G与Br2的CCl4溶液反应,产物有 种(不考虑立体异构)。
(2)反应②的化学方程式为 。
(3)E可在一定条件下通过 (填反应类型)生成高分子化合物,写出该高分子化合物可能的结构简式: (两种即可)。
(4)反应⑥的化学方程式为 。
(5)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,写出所有符合条件的Y的结构简式: 。Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是( )
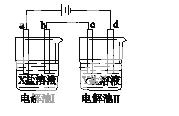
| 选项 | X | Y |
| A. | MgSO4 | CuSO4 |
| B. | AgNO3 | Pb(NO3)2 |
| C. | FeSO4 | Al2 (SO4)3 |
| D. | CuSO4 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为第________周期、第________族;PbO2的酸性比CO2的酸性________(填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_______________________。
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___________________;PbO2也可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生的电极反应式为____________________,阴极上观察到的现象是____________________;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为______________________________,这样做的主要缺点是____________________。
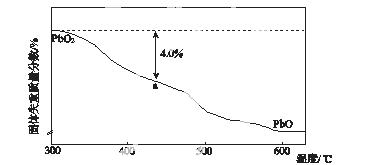
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%(即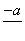 ×100%)的残留固体。若a点固体组成
×100%)的残留固体。若a点固体组成 表示为PbOx或mPbO2·nPbO,列式计算x值和m∶n值________________________________________。
表示为PbOx或mPbO2·nPbO,列式计算x值和m∶n值________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极进行下列电解,有关说法正确的是( )
①电解稀硫酸 ②电解CuSO4溶液 ③电解KOH溶液 ④电解NaCl溶液
A.电解进行一段时间后四份溶液的pH均增大
B.②中电解一段时间后,向溶液中加入适量的CuO固体可使溶液恢复电解前的情况
C.③中阳极消耗OH-,故溶液浓度变小
D.④中阴、阳两极上产物的物质的量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
某可逆反应平衡常数表达式为K= 。达到平衡状态时,如果升高温度(其他条件不变),则c(NO)减小。下列说法正确的是
。达到平衡状态时,如果升高温度(其他条件不变),则c(NO)减小。下列说法正确的是
( )
A.反应的热化学方程式为NO2(g)+SO2(g)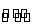 NO(g)+SO3(g) ΔH>0
NO(g)+SO3(g) ΔH>0
B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深
C.混合气体的平均摩尔质量保持不变,说明反应已达平衡
D.使用合适的催化剂可使该反应的反应速率和平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是 10ml 量筒的一部分,数字XY之间相差 2mL
若 X=6,则量筒所盛液体的体积是
A. 5.2 ml B. 4.3 ml C.4.6 ml D.7.4 ml
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢键,下列说法正确的是
A.由于冰中的水分子间存在氢键,所以其密度大于液态水
B.可以用氢键解释接近沸点的水蒸气的相对分子质量测定值比用化学式(H2O)计算出来的相对分子质量大
C.分子间氢键和分子内氢键都会使熔沸点升高
D.水加热到很高的温度都难以分解,这是由于氢键所致
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com