
科目:高中化学 来源: 题型:选择题
| A. | 五价砷在维生素C作用下发生了还原反应 | |
| B. | “两者同食”发生的反应中维生素C作还原剂 | |
| C. | 河虾中含有的五价砷,没有毒性 | |
| D. | 毒药砒霜是含砷的氧化物,可以推测砒霜中所含的砷元素化合价为+5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2→MgO | B. | Fe3O4→H2O | C. | FeCl3→CuCl2 | D. | MnO2→Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe-Zn合金 | B. | Fe-Cu合金 | C. | Fe-Mg合金 | D. | Mg-Al合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
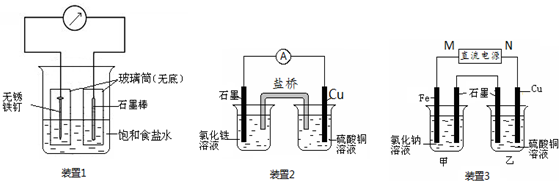
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L | |
| B. | 标况下,22.4L空气中含有NA个单质分子 | |
| C. | 1molCl2参加反应转移电子数一定为2NA | |
| D. | 在18g18O2中含有10NA个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3+2HCl═CaCl2+CO2↑+H2O | B. | CaO+H2O═Ca(OH)2 | ||
| C. | 2Na2O2+2CO2═2Na2CO3+O2 | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com