


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.锂为电池的正极,石墨作电池的负极 |
| B.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 |
| C.电解质溶液中混入水,对电池反应无影响 |
| D.电池工作过程中,锂提供的电子与正极区析出硫的物质的量之比为4:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2PbSO4 +2H2O。请依据上述情况判断:⑴铅蓄电池的负极材料是 。
2PbSO4 +2H2O。请依据上述情况判断:⑴铅蓄电池的负极材料是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| ||
| ||
| A.该电池的工作环境是高温条件 | ||||
| B.葡萄糖(C6H12O6)在变化中失去电子,被还原 | ||||
| C.该电池的电解质溶液是强酸性溶液,如浓硫酸等 | ||||
D.该电池的总反应式为C6H1206+602
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
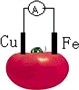
| A.铜片为负极 |
| B.铁片上发生还原反应 |
| C.该装置将电能转变为化学能 |
| D.电子由铁片沿导线流向铜极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.每生成1 mol Na2Mn5O10转移2 mol电子 | B.正极反应式:Ag+Cl--e-=AgCl |
| C.Na+不断向“水”电池的负极移动 | D.AgCl是还原产物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com