
| A、1L 0.1mol/L次氯酸溶液中离子总数为0.2NA |
| B、标准状况下22.4 L SO3 中含氧原子数为3NA |
| C、1mol过氧化氢中含有3NA个共价键 |
| D、常温下,1molFe与足量浓硫酸反应失去3NA个电子 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
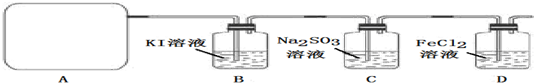

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧菜用过的铁锅,经放置常出现红棕色斑迹 |
| B、用煤气灶燃烧沼气[主要成分为甲烷(CH4中C为-4价)]为炒菜提供热量 |
| C、利用漂白粉漂白有色物质 |
| D、食醋除热水瓶中的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在3.4gNH3中,含有N-H键为0.6NA |
| B、在标准状况下,体积为22.4L的己烷完全燃烧后,所生成气态产物的分子数为6NA |
| C、16gO2在反应中做氧化剂时转移的电子个数一定是2NA |
| D、在标准状况下,46gNO2和N2O4混合物所含分子个数是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠投入水中 |
| B、石墨在高温高压下转化为金刚石 |
| C、干冰汽化 |
| D、氯化铵受热会挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:
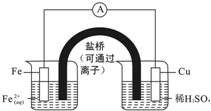
| A、电子由Cu电极流向Fe电极 |
| B、盐桥中的阳离子移向左池 |
| C、Fe电极为负极,Cu电极为正极 |
| D、Cu电极的电极反应式为:Cu-2e-=Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有机物A的名称为α-羟基丁酸 |
| B、有机物B的结构简式可能为CH3CH=CHCOOH |
| C、有机物C和D属同分异构体 |
| D、环状有机物E的结构只有一种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com