
【题目】下列表示式错误的是( )
A.Mg2+的电子排布图: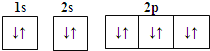
B.Na+的结构示意图:![]()
C.Cr的价层电子排布式:3d54s1
D.C的电子排布式:1s22s12p3
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6![]() 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ.已知:实验室制乙烯原理为CH3CH2OH![]() CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
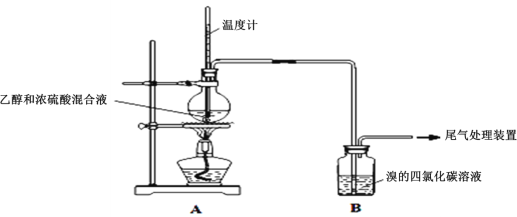
操作 | 现象 |
点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
…… | |
实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有___性。
(2)对产生的气体进行分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①写出实验室制取SO2的化学反应方程式是___;
②乙根据现象认为实验中产生的SO2和___,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)
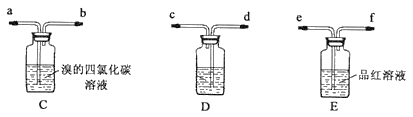
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是___;乙设计的实验D中盛放的试剂是___,装置连接顺序为___ (用仪器接口字母编号)。
b.能说明确实是SO2使E中溶液褪色的实验是___。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是___。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色。
Ⅱ.葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时溶液中离子浓度由大到小的排列顺序___。
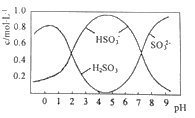
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤___mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体([CH3CH(OH)COO]2Fe·3H2O,Mr=288) 可由乳酸与FeCO3反应制得,它易溶于水,是一种很好的补铁剂。
Ⅰ.制备碳酸亚铁(装置如图所示)
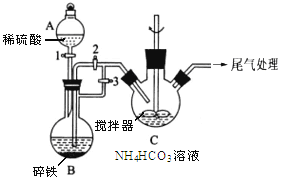
(1)仪器A的名称是______________ ;
(2)实验操作如下:关闭活塞2,打开活塞1、3,加入适量稀硫酸反应一段时间,其目的是___________________________________________________________;然后关闭活塞1,接下来的操作是_______________; 装置C中发生反应的离子方程式为______________ 。
Ⅱ.制备乳酸亚铁
向纯净的FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应。
(3)为防止乳酸亚铁变质,在上述体系中还应加入____________________________________________________________________________
(4)为证明乳酸亚铁中含有Fe2+,选择的检验试剂为_______________________________________________________________________;
Ⅲ. 乳酸亚铁晶体纯度的测量
经过过滤、隔绝空气低温蒸发、冷却结晶、过滤、洗涤、干燥等操作,获得乳酸亚铁晶体后
(5)两位同学分别用不同的方案进行测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度,所得纯度总是大于100%,其原因可能是_________________________________________________________________________________________________________________
②乙同学经查阅文献后改用(NH4)4Ce(SO4)4滴定法测定样品中Fe2+的含量计算样品纯度(反应中Ce4+被还原为Ce3+),称取6.00g样品配成250.00mL溶液,取25mL,用0.1 molL—1(NH4)4Ce(SO4)4标准溶液滴定至终点,消耗标准液20.00mL。则产品中乳酸亚铁晶体的纯度为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.1molL﹣1的H2A(二元弱酸)溶液中滴加0.1mol/L的NaOH溶液,溶液pH随NaOH溶液体积的变化如图所示。下列说法正确的是
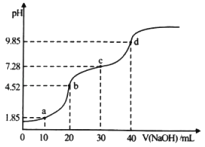
A.a点的溶液中:c(Na+)>c(A2)>c(HA)>c(H+)>c(OH)
B.b点的溶液中:c(H2A)+c(H+)=c(A2)+c(OH)
C.c点溶液的pH>7,是因为此时HA的电离能力小于其水解能力
D.若将0.1molL﹣1的NaOH溶液换成同浓度的氨水,当滴加40mL时,此时溶液的pH>9.85
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以检验某品牌茶叶中铁元素的存在并测定钙元素的质量分数(已知CaC2O4为白色沉淀物质)。首先取200g茶叶样品进行如图操作:
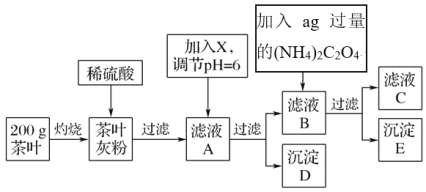
已知:①文献资料显示:某些金属离子的氢氧化物完全沉淀时的pH为:Ca(OH)2:13,Fe(OH)3:4.1
②(NH4)2C2O4溶液显酸性。
(1)实验前要先将茶叶样品高温灼烧为灰粉,需要用到的实验仪器有酒精灯、三脚架、玻璃棒、泥三角________,其主要目的是___________________。
A.蒸发皿 B.坩埚C.石棉网
(2)从滤液A→沉淀D的过程中需要加入的物质X可以选择________。
A.CaO B.Ca(OH)2C.NH3·H2O
(3)用酸性KMnO4标准溶液滴定滤液C时发生的反应为:5C2O42-+2MnO4-+16H+===10CO2↑+2Mn2++8H2O。将滤液C稀释至250mL,取25.00mL溶液,用硫酸酸化后,用0.10mol·L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液体积如表所示:
编号 | KMnO4溶液体积/mL |
1 | 19.98 |
2 | 22.00 |
3 | 20.02 |
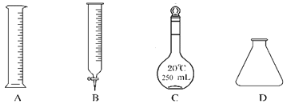
①此步操作过程中需要用到图示中哪些仪器________
②滴定达到终点时的现象是__________________________。
③为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,若不洗涤沉淀D,会使测定的钙元素的含量________(偏低、偏高、无影响,下同),若不洗涤沉淀E,会使测定的钙元素的含量________。
④原茶叶中钙元素的质量分数为________。(用含a的代数式表示,已知(NH4)2C2O4的摩尔质量为124g·mol-1)。
(4)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及实验现象是_______________、________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图(如图),回答下列问题。

(1)操作Ⅰ中所用的仪器有____。
(2)固体A的成分是___和____。(填名称);操作Ⅲ是____。
(3)如何检验溶液a中主要阴离子____。
(4)回收的铜可以用于制备胆矾(CuSO4·5H2O)。将铜和0.22mol/LH2SO4溶液混合后,在加热的情况下不断通入氧气就可以制得CuSO4,然后将所得的溶液经过“一系列操作”后得到胆矾。写出生成CuSO4的化学方程式:___。
(5)某同学用密度为1.84g/cm3、质量分数为 98%的浓硫配制500mL0.22mol/L的稀硫酸溶液,需要用规格为___mL的量筒量取___mL的浓硫酸。
(6)配制该溶液的过程中,下列操作使得所配得的溶液浓度偏小的是___(填字母)。
A.稀释密度为1.84g/cm3、质量分数为 98%的浓硫酸时,不小心溅出少量硫酸溶液
B.用蒸馏水洗涤烧杯、量筒及玻璃棒,并将洗涤液注入容量瓶中
C.定容时反复上下倒转容量瓶后,发现凹液面最低处低于刻度线,再补加水到刻度线
D.量取密度为1.84g/cm3、质量分数为 98%的浓硫酸时,仰视量筒的刻度线
E.洗涤容量瓶后,立即用来配制溶液
F.稀释浓硫酸结束后立即将溶液转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。
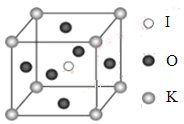
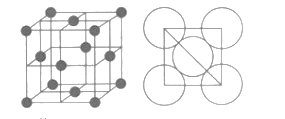
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
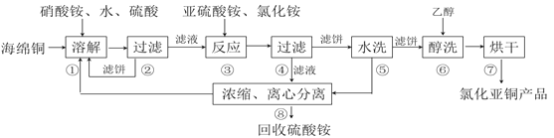
回答下列问题:
(1)步骤①中得到的氧化产物是_________,溶解温度应控制在60~70度,原因是__________。
(2)写出步骤③中主要反应的离子方程式___________。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是______________________________。
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有__________(填字母)
A.分馏塔 | B.离心机 | C.反应釜 | D.框式压滤机 |
(6)准确称取所制备的氯化亚铜样品m g,将其置于若两的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳硫、铝、铁是生活中常见的四种元素,根据所学知识回答下列问题:
(1)铁原子基态时核外电子排布式为__,三氯化铁的熔点306℃、沸点315℃,由此判断三氯化铁属于___晶体。
(2)碳的电负性比硫__(填“大”“小”或“相等"),碳、氮、氧元素第一电离能由大到小的顺序为__(填元素符号)。
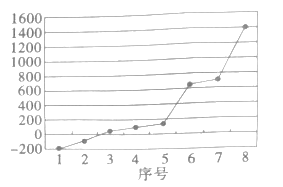
(3)硫元素所在周期的8种元素的单质熔点如图所示,其中序号“8”代表__(填元素符号);形成最高价氧化物对应水化物酸性最强的是__(填图中的序号)。
(4)CS2分子的空间构型为__,C原子的价层电子对数为__。
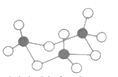
(5)固态SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为__;该分子中含有___个σ键。
(6)铝单质的晶胞特征及原子之间相互位置关系如图所示,若已知铝的原子半径为dcm,NA代表阿伏加德罗常数,铝的相对原子质量为M,则该晶体的密度为__g/cm3(用字母表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com