
| A、①② | B、②③ | C、③④ | D、①③ |
| y |
| 4 |
| z |
| 2 |
| y |
| 2 |
| y |
| 4 |
| z |
| 2 |
| y |
| 4 |
| z |
| 2 |
| y |
| 2 |
| y |
| 4 |
| z |
| 2 |


科目:高中化学 来源: 题型:
 Ⅰ:工业上用CO2和H2在一定条件发生如下反应合成甲醇并放出大量的热:CO2(g)+3H2(g)?CH3OH(g)+、H2O(g)△H1 回答下列问题.
Ⅰ:工业上用CO2和H2在一定条件发生如下反应合成甲醇并放出大量的热:CO2(g)+3H2(g)?CH3OH(g)+、H2O(g)△H1 回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
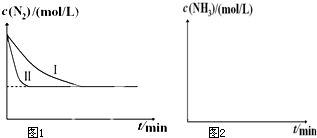 (1)已知:N2(g)+O2(g)═2NO(g)△H1
(1)已知:N2(g)+O2(g)═2NO(g)△H1| 温度/℃ | 起始量/mol | 平衡量/mol[学科 | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
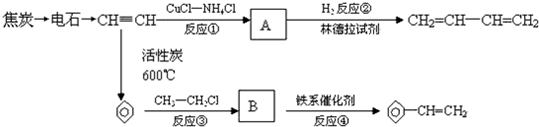
查看答案和解析>>
科目:高中化学 来源: 题型:
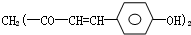 它制成的试纸可以检验酸碱性,能够跟1mol该化合物起反应的NaOH和H2的最大量分别为( )
它制成的试纸可以检验酸碱性,能够跟1mol该化合物起反应的NaOH和H2的最大量分别为( )| A、3mol,3mol |
| B、1mol,5mol |
| C、6mol,8mol |
| D、2mol,10mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n(A)=n(C) |
| B、n(B)=n(C) |
| C、n(A)+n(B)=n(C) |
| D、n(B)+n(C)=n(A) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 4 |
| 5 |
| A、50% | B、37.5% |
| C、25% | D、12.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:
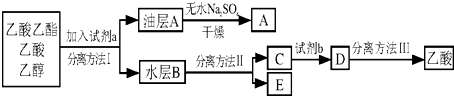
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com