
(10分)A—K是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末,G、H为气态单质,I在常温下为液体,D、E、F的水溶液均呈碱性,由C的饱和溶液制取F或E是重要的化工生产。回答下列问题: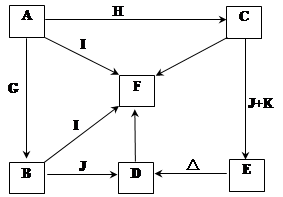
(1)写出下列物质的化学式:C________E_______
(2)写出下列反应的化学方程式: B D:_______________________________
B D:_______________________________ C E:_______________________________
C E:_______________________________
(3)画出F的电子式:________________
(4)常温下若电解1L C的饱和溶液,当电路中通过0.1mol电子时,溶液的pH值(假设溶液体积不变)为_________。
(1)NaCl、NaHCO3
(2)B D:2Na2O2+2CO2=2Na2CO3+O2 C E:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
(3)  (4)13
(4)13
解析试题分析:B为淡黄色粉末,B为Na2O2,则A为Na,G为O2,又知I在常温下为液体,I为H2O,F为NaOH。因为能与Na2O2反应的物质除了水还有CO2,则J为CO2,D为Na2CO3,E为NaHCO3。由C的饱和溶液制取F或E是重要的化工生产,所以C是NaCl,H为Cl2,K为NH3。
常温下若电解1LNaCl溶液,当电路中通过0.1mol电子时,说明溶液中有0.1molH+放电,因此溶液中产生OH-0.1mol,则溶液中c(OH-)=0.1mol/L,溶液的pH为13。
考点:无机框图
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。


 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源:2013届吉林长春实验中学高二下学期期末考试化学试卷(解析版) 题型:填空题
(10分)A—K是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末,G、H为气态单质,I在常温下为液体,D、E、F的水溶液均呈碱性,由C的饱和溶液制取F或E是重要的化工生产。回答下列问题:

(1)写出下列物质的化学式:C________E_______
(2)写出下列反应的化学方程式:
B D:_______________________________
 C
E:_______________________________
C
E:_______________________________
(3)画出F的电子式:________________
(4)常温下若电解1L C的饱和溶液,当电路中通过0.1mol电子时,溶液的pH值(假设溶液体积不变)为_________。
查看答案和解析>>
科目:高中化学 来源:2014届湖北省武汉市五校高一下学期期中统考化学试卷(解析版) 题型:填空题
(10分)
|
A |
|
|
|||||||||||||||||||||||
|
B |
|
|
|
C |
D |
E |
F |
|
|||||||||||||||||
|
G |
|
H |
|
|
|
I |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
(1)在上面元素周期表中全部是金属元素的区域为___________。
A.a B.b C.c D.d
(2)G元素单质在E元素单质中燃烧时形成的化合物的化学式是______,它是__________(填“共价化合物”或“离子化合物”)。该化合物含有的化学键类型是 ;
该化合物的电子式是 。
(3)表格中九种元素能形成最高价氧化物对应的水化物中,碱性最强的是________(用化合物的化学式表示,下同),酸性最强的是__________,属于两性氢氧化物的是__________。
(4)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 ________(填名称),可以验证该结论的实验是_______。(填编号)
a将在空气中放置已久的这两种元素的块状单质分别放入热水中;
b将这两种元素的单质粉末分别和同浓度的盐酸反应;
c将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液;
d比较这两种元素的气态氢化物的稳定性。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ(10分) A、B、C、D四种元素在周期表中分别处于元素X的四周(如下图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的。试确定:
(1)各元素的符号:
A:_____,B:____,C:____,D:_____,X:_____。
(2)写出C、D、X最高价氧化物对应水化物的化学式,并排列酸性由强到弱的顺序:___________。
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:__________________。
Ⅱ(8分)Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+![]() 2Fe2++I2(水溶液),
2Fe2++I2(水溶液),
⑴该反应的平衡常数K的表达式为:K= ___________________________
[物质的浓度用“c(物质)”表示]。当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡________移动(填“向右”、“向左”、“不”)。
⑵上述反应的正向反应速率和I-、Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+)]n(其中K为常数)
| c(I-)(mol/L) | c(Fe3+)(mol/L) | v[mol/(L?s)] | |
| ⑴ | 0.20 | 0.80 | 0.032K |
| ⑵ | 0.60 | 0.40 | 0.144K |
| ⑶ | 0.80 | 0.20 | 0.128K |
通过所给的数据计算得知:
①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为_________。
A. m=1、n=1 B. m=1、n=2 C. m=2、n=1 D. m=2、n=2
②I-浓度对反应速率的影响_______Fe3+浓度对反应速率的影响(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分) A到K为中学常见物质,B是一种能使湿润的红色石蕊试纸变蓝的气体,F遇空气变为红棕色,反应③是实验室制备B气体的常用反应,它们之间的转化关系如下图所示(其中某些反应条件和部分反应产物已略去)。回答下列问题:

(1)A的化学式 ▲ 。
(2)在反应①—⑤中,有电子转移的反应是 ▲ (填编号)。
(3)实验室制备B的化学方程式 ▲ 。
(4)试写出反应④的离子反应方程式: ▲ ;
(5)J与金属Cu反应表现的性质为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com