
【题目】下列变化中,需加入适当的还原剂才能完成的是( )
A.KI→I2
B.FeCl2→FeCl3
C.CuO→Cu
D.CO2→Na2CO3
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质,在室温下A为固体,B和C为气体,向D溶液中加入KSCN溶液后,溶液显红色。在适宜的条件下可发生如下关系的化学反应。
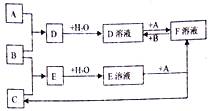
回答以下问题:
(1)写出B的化学式:____________
(2)写出E溶液和+A→F溶液+C的离子反应方程式:___________________。D溶液和+A→F溶液的离子反应方程式:_______________________________。若向F溶液中加入NaOH溶液,观察到的现象为:________________________。
(3)写出除去D溶液中F杂质的离子反应方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
(1)利用工业废气 CO2 可制取甲醇。 下列两个反应的能量关系如图:
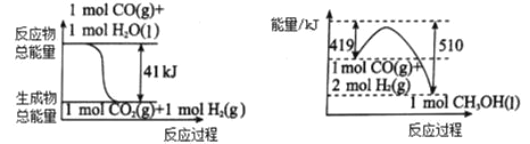
则 CO2与 H2 反应生成 CH3OH 的热化学方程式为_______________________。
(2)CH4 和 H2O(g)通过下列转化也可以制得 CH3OH;
I. CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
II. CO(g)+2H2(g) ![]() CH3OH(g) △H<0
CH3OH(g) △H<0
将 1.0 mol CH4和 3.0 mol H2O(g)通入反应室(容积为 100 L)中,在一定条件下发生反应 I, CH4 的转化率与温度、压强的关系如下图所示:
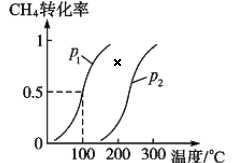
①已知压强 p1, 温度为 100 ℃时反应 I 达到平衡所需的时间为 5 min,则用 H2表示的平均反应速率为______________;
②图中的 p1_______p2(填“<”、 “>”或“=”),判断的理由是________________________。
③若反应 II 在恒容密闭容器进行,下列能判断反应 II 达到平衡状态的是_________(填字母)。
a.CH3OH 的生成速率与消耗 CO 的速率相等
b.混合气体的密度不变
c混合气体的总物质的量不变
d.CH3OH、CO、H2的浓度都不再发生变化
④ 在某温度下,将一定量的CO和 H2投入10 L 的密闭容器中发生反应 II, 5 min 时达到平衡,各物质的物质的浓度(mol·L ﹣1)变化如下表所示:
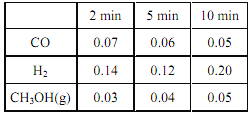
若 5 min 时只改变了某一条件,则所改变的条件是_____________; 10 min 时测得各物质浓度如上表,此时 v正_______v逆(填“<”、 “>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时红磷比白磷稳定,在下列反应中:
4P(白磷,s)+5O2(g)====2P2O5(s);△H=== -a kJ/mol
4P(红磷,s)+5O2(g)====2P2O5(s);△H=== -b kJ/mol
若a、b均大于零,则a和b的关系为
A.a<bB.a=bC.a>bD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、密闭容器中投入一定量的CaCO3发生分解反应:CaCO3(s)![]() CaO(s)+CO2(g) ΔH>0。达到平衡时,测得体系中气体的压强为P。若温度不变,缩小体积至原来的一半,重新达到平衡。下列说法不正确的是( )
CaO(s)+CO2(g) ΔH>0。达到平衡时,测得体系中气体的压强为P。若温度不变,缩小体积至原来的一半,重新达到平衡。下列说法不正确的是( )
A. 当CaCO3的浓度不再变化时,表明达到平衡状态
B. 重新达到新平衡时,CO2的压强为P
C. 扩大容器体积,重新达到平衡时n(CO2)增多
D. 常温常压下CaCO3的分解反应不一定自发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏伽德罗常数的值,下列说法正确的是
A. 2.8 g铁与0.05 mol Cl2充分反应,转移0.15NA电子
B. 27 g Al与足量NaOH溶液反应生成33.6 L H2
C. 14 g由乙烯(C2H4)和丙烯(C3H6)组成的混合物中含有原子的数目为3NA
D. 300 mL 0.2 mol/L蔗糖溶液中所含分子数为0.06NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在生产、生活和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布图为______________。
(2)在氮分子中,氮原子之间存在着______个σ键和______个π键。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣,请写出两种与N3﹣互为等电子体的分子_______ 、_______。
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是_____________________。
(5)NF3、NCl3、NBr3的沸点由高到低的顺序是___________________________。
(6)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体.该反应的化学方程式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com