
| A. | 常温下pH=5的盐酸溶液稀释103倍后,pH等于8 | |
| B. | 浓度均为0.1mol/L的氨水和氯化铵溶液,水电离出的c(H+)前者小于后者 | |
| C. | Na2CO3溶液中存在:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 常温下,pH=2的CH3COOH溶液与pH=12的KOH溶液等体积混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
分析 A.酸无限稀释不能变成碱溶液或中性溶液,只能是接近中性溶液;
B.酸或碱抑制水电离,含有弱离子的盐促进水电离;
C.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
D.常温下,pH=2的醋酸溶液浓度大于pH=12的KOH溶液,二者等体积混合,醋酸有剩余,溶液呈酸性,溶液中存在电荷守恒.
解答 解:A.酸无限稀释不能变成碱溶液或中性溶液,只能是接近中性溶液,所以常温下pH=5的盐酸稀释100倍时溶液pH接近7,故A错误;
B.酸或碱抑制水电离,含有弱离子的盐促进水电离,一水合氨抑制水电离、氯化铵促进水电离,所以水电离出的c(H+)前者小于后者,故B正确;
C.任何电解质溶液中都存在物料守恒,根据物料守恒得c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)],故C错误;
D.常温下,pH=2的醋酸溶液浓度大于pH=12的KOH溶液,二者等体积混合,醋酸有剩余,溶液呈酸性,溶液中存在电荷守恒,根据电荷守恒得c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确;
故选BD.
点评 本题考查离子浓度大小比较,明确溶液中的溶质及其性质是解本题关键,利用电荷守恒、物料守恒判断,易错选项是A,酸或碱无限稀释接近中性时要考虑水的电离.


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
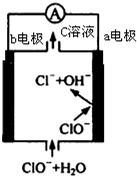 镁-次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO -+H2O═Mg(OH)2+Cl-下列有关说法正确的是( )
镁-次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO -+H2O═Mg(OH)2+Cl-下列有关说法正确的是( )| A. | 电池工作时,C溶液中的溶质是MgCl2 | |
| B. | 电池工作时,正极a附近的PH将不断增大 | |
| C. | 负极反应式:ClO --2e -+H2O═Cl-+2 OH- | |
| D. | b电极发生还原反应,每转移0.1mol电子,理论上生成0.1mol Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |
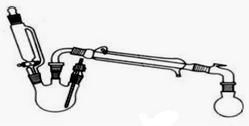
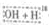 OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
 后消去失水,失水有两种可能分别生成
后消去失水,失水有两种可能分别生成 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )| A. | 羟基硝酸铵中阳离子的各原子共平面 | |
| B. | 羟基硝酸铵是离子化合物 | |
| C. | 羟基硝酸铵中含有离子键和共价键 | |
| D. | 9.6g羟基硝酸铵中含有0.2mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;反应③
;反应③ .
.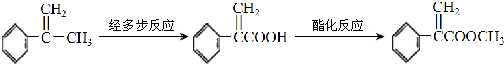
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L NO和O2混合气体的原子数为NA | |
| B. | 15g甲基所含有的电子数目为9NA | |
| C. | 1L0.1mol/L的氨水溶液中含有的N原子数大于0.1NA | |
| D. | 标准状况下,6.72L NO2与水反应转移电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C12H20O2 | |
| B. | 能发生加成反应、取代反应、氧化反应 | |
| C. | 1mol该有机物在一定条件下能和3mol H2发生反应 | |
| D. | 该有机物仅含有两种不同类型的官能团 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com