
分析 根据浓硫酸增重的为水的质量,氢氧化钠增重的为二氧化碳的质量,根据n=$\frac{m}{M}$计算出水、二氧化碳的物质的量,从而得出芳香烃的分子中含有的C、H原子数,确定其的分子式及结构简式.
解答 解:苯的同系物完全燃烧生成的气体通过浓硫酸和氢氧化钠时,浓硫酸吸收水蒸气,氢氧化钠吸收二氧化碳,故0.1mol苯的同系物燃烧生成水7.2g,二氧化碳30.8g,则n(H2O)=$\frac{7.2g}{18g/mol}$=0.4mol,根据原子守恒知,n(H)=2n(H2O)=0.8mol,n(CO2)=$\frac{30.8g}{44g/mol}$=0.7mol,所以n(苯的同系物):n(C):n(H)=0.1mol:0.7mol:0.8mol=1:7:8,苯的同系物的分子式为:C7H8,其结构简式为 ;
;
故答案为:C7H8, .
.
点评 本题考查了有机物分子式、结构式的确定,题目难度中等,注意掌握确定有机物分子式的方法,试题培养了学生灵活应用所学知识的能力.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
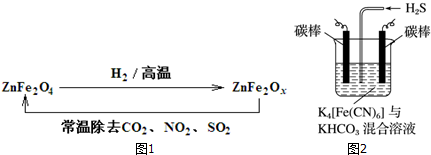
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
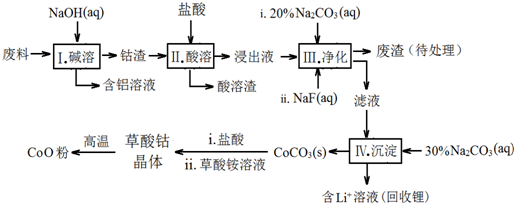
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
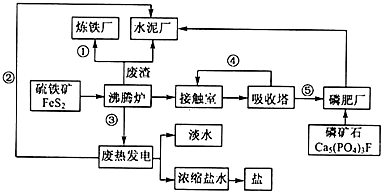 生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图.
生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
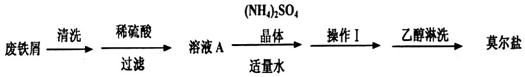
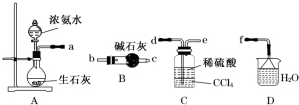
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
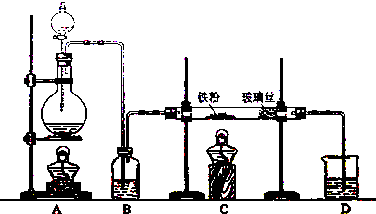
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15g甲基(-CH3)所含有的电子数是NA | |
| B. | 常温常压下,4g氦气所含有的原子数目为NA | |
| C. | 标准状况下,1L己烷充分燃烧后生成的气态产物的分子数为$\frac{6}{22.4}$NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com