
【题目】原油价格的下跌,加剧能源的过度开采,因此更要开展汽油的有机合成的研究。以下是一种合成汽油的路线:

已知:R-CH2-CHO+R1-CH2-CHO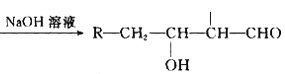
2R-CH2-Cl+2Na![]() R-CH2-CH2-R+2NaCl
R-CH2-CH2-R+2NaCl
CH3-CH=CH2+H-Cl
请根据以上信息回答下列问题:
(1)在反应①—⑥中,属于加成反应的是_________,B的分子式为 ________。
(2)A中官能团名称为_________, E的名称为 ____________。
(3)写出下列反应方程式:E→F_____________________H→G_________________。
(4)H也能与NaOH溶液反应,其反应方程式为:_________________________。
(5)D的核磁共振氢谱有____组吸收峰。写出符合下列条件D的所有同分异构体___________。
①链状结构,②能与钠反应生成气体,③不饱和碳上不与含氧官能团直接相连。
【答案】①③⑤ CH4O 醛基 2-甲基-1-丙醇  +H2O
+H2O  +2NaCl
+2NaCl  +NaCl 3 CH≡CCH2CH2OH、CH3C≡CCH2OH、CH≡CCHOHCH3
+NaCl 3 CH≡CCH2CH2OH、CH3C≡CCH2OH、CH≡CCHOHCH3
【解析】
B氧化得甲醛,所以B为甲醇,乙炔加成得A为CH3CHO,甲醛与丙醛发生信息中的反应生成C为HOCH2CH(CH3)CHO,根据D的分子式可知,C在浓硫酸作用下加热发生消去反应生成D为CH2=C(CH3)CHO,D与氢气加成得E为(CH3)2CHCH2OH,E在浓硫酸加热的条件下发生消去反应得F为(CH3)2C=CH2,F与氯化氢发生信息中的反应得H为(CH3)2CClCH3,H与钠发生信息中反应得G为(CH3)3CC(CH3)3,据此答题。
(1)根据上面的分析可知,在反应①-⑥中,属于加成反应的是①③⑤,B为甲醇,故答案为①③⑤;CH4O;
(2)A为CH3CHO,官能团名称为醛基,E为(CH3)CHCH2OH,E的名称为2-甲基-1丙醇,故答案为:醛基;2-甲基-1丙醇;
(3)E→F的反应方程式为 +H2O ;H→G的反应方程式为
+H2O ;H→G的反应方程式为 +2NaCl;
+2NaCl;
(4)H与氢氧化钠反应的化学方程式为 +NaCl
+NaCl
(5)D为CH2=C(CH3)CHO,分子中有3种化学环境不同的氢原子,D的核磁共振氢谱有3组吸收峰,根据题目中的已知条件,符合要求的同分异构体有3种,分别是CH≡CCH2CH2OH、CH3C≡CCH2OH、CH≡CCHOHCH3,故答案为:3;CH≡CCH2CH2OH、CH3C≡CCH2OH、CH≡CCHOHCH3。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁发给来自美国、英国、日本的三位科学家,表彰他们在锂离子电池方面的研究贡献。锂离子电池广泛应用要求处理锂电池废料以节约资源、保护环境。锂离子二次电池正极铝钴膜中主要含有钴酸锂(LiCoO2)、Al等,处理该废料的一种工艺如下图所示:

回答下列问题:
(1)铝钴膜在处理前初步进行粉碎的目的是________________________。
(2)能够提高“碱浸”效率的方法有________________________(至少写两种)。
(3)“碱浸”时Al溶解的离子方程式为________________________。
(4)“酸溶”时加入H2O2的目的是________________________。
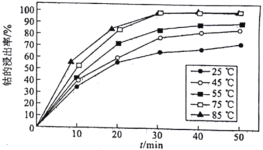
(5)溶液温度和浸渍时间对钴的浸出率影响如图所示,则浸出过程的最佳条件是_______________________。
(6)配制250 mL 1.0 mol/L (NH4)2C2O4溶液,需要的玻璃仪器除玻璃棒、烧杯外还需要________。
(7)取CoC2O4固体4.41g在空气中加热至300℃,得到钴的氧化物2.41g,则该钴的氧化物的化学式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为比较镁、铝的金属性强弱,设计了如下实验:
(1)向两支试管中分别加入3mL同浓度的稀盐酸,再将两块大小相同且纯净的镁片和铝片分别加入试管中,反应完全后观察到如图所示的现象,则试管b内加入的金属为____________(写化学式)。

(2)若加入的两块金属的物质的量相等,且试管中稀盐酸足量,充分反应后,气球状态也如图所示,则试管b中反应的离子方程式为____________。
(3)分析判断,实验________[填“(1)”或“(2)”]能证明镁的金属性强于铝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氯乙酮是一种具有荷花香味且有强催泪作用的杀伤性化学毒剂,它的结构简式如图所示,下列说法错误的是

A.分子式为C8H7OClB.在同一平面上的碳原子最多有8个
C.1mol苯氯乙酮最多可与3molH2发生加成反应D.核磁共振氢谱有4个吸收峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是![]()
![]()
①质子数相同的微粒一定属于同一种元素![]()
②同位素的性质相同![]()
③质子数相同、电子数也相同的微粒,不可能是一种分子和一种离子![]()
④电子数相同的微粒不一定是同一种元素![]()
⑤一种元素只能有一种质量数![]()
⑥某种元素的相对原子质量取整数,就是其质量数![]()
⑦![]() 中
中![]() 与
与![]() 的原子个数之比与NaCl中的
的原子个数之比与NaCl中的![]() 与
与![]() 的原子个数之比相等
的原子个数之比相等
A.②③⑤⑥⑦B.①②④⑤C.①②⑤⑥D.③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微粒A的结构示意图为![]()
(1)若A是原子,则A的元素符号为__;若A是带一个正电荷的阳离子,则X=___
(2)若X=8,则此阴离子与(1)中带一个正电荷的阳离子形成一种常见化合物的化学式是___,它是不是电解质(填是或否)____。写出此化合物与盐酸反应的化学方程式:________________________________
(3)1mol微粒A含有10mol电子,下列微粒各1mol,也含有10mol电子的有:___(填序号)
①CH4 ②H2O2 ③HF ④Al3+ ⑤Cl- ⑥NH4+
(4)若A的阳离子为An+且质量数为a,则其质子数为____________,中子数为_______________(用含有a,n的代数式表达)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出表示含有8个质子,10个中子的原子的化学符号:______;
(2)最外层电子数为次外层电子数![]() 的原子______或______;(填元素符号)
的原子______或______;(填元素符号)
(3)根据下列微粒回答问题:
![]() H、
H、![]() H、
H、![]() H、
H、![]() C、
C、![]() 、
、![]() 、
、![]() 、
、![]()
①以上8种微粒共有______种核素,共______种元素.
②互为同位素的是______.
③质量数相等的是______和______,中子数相等的是______和______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸在溶剂中的电离实质是酸中的H+转移给溶剂分子,如HCl+H2O=H3O++Cl-。已知H2SO4和HNO3在冰醋酸中的电离平衡常数分别为Kal(H2SO4)=6.3×10-9,Ka(HNO3)=4.2×10-10。下列说法正确的是( )
A.H2SO4在冰醋酸中的电离方程式为H2SO4+2CH3COOH=SO42-+2CH3COOH2+
B.H2SO4在冰醋酸中:![]() =c(HSO4-)+2c(SO42-)+c(CH3COO-)
=c(HSO4-)+2c(SO42-)+c(CH3COO-)
C.浓度均为0.1mol·L-1的H2SO4或HNO3的冰醋酸溶液:pH(H2SO4)>pH(HNO3)
D.向HNO3的冰醋酸溶液中加入冰醋酸, 的值减小
的值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述不正确的是
A.立方烷( )的二氯代物有3种,三氯代物也有3种
)的二氯代物有3种,三氯代物也有3种
B.有机物 (CH3)2CHC(CH3)3的名称为2,2,3三甲基丁烷
C.向鸡蛋清的溶液中加入浓的硫酸钾溶液或福尔马林,蛋白质的性质发生改变并凝聚
D.用CH2(NH2)—COOH和CH3—CH(NH2)—COOH两种氨基酸脱水,最多可以生成4种二肽
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com