
| A. | 溶解度:小苏打<苏打 | B. | 沸点:K>Na | ||
| C. | 密度:溴>水 | D. | 热稳定性:HF>HCl |
分析 A.相同条件下,碳酸钠溶解度大于碳酸氢钠;
B.随着原子序数的递增,碱金属单质的沸点逐渐减小;
C.溴的密度大于水;
D.非金属性越强,对应氢化物的稳定性越强.
解答 解:A.在碳酸钠饱和溶液中通入二氧化碳生成碳酸氢钠,可观察到溶液变浑浊,说明碳酸钠溶解度大于碳酸氢钠,故A正确;
B.K、Na位于同一主族,原子序数K>Na,则沸点:K<Na,故B错误;
C.溴的密度比水大,即密度:溴>水,故C正确;
D.非金属性F>Cl,则对应氢化物的稳定性:HF>HCl,故D正确;
故选B.
点评 本题考查元素及其对应单质、化合物的性质的递变规律,侧重于溶解度、沸点、密度、热稳定性等性质的考查,题目难度不大,注意把握性质比较的角度以及规律.


科目:高中化学 来源: 题型:解答题
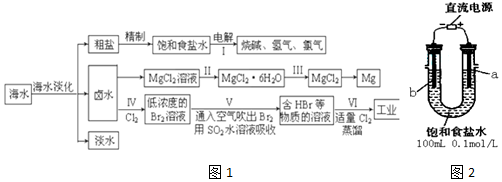
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
| 完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
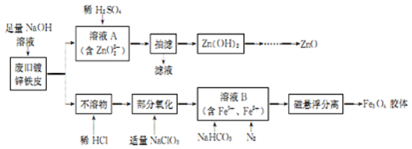
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H4=$\frac{3}{2}$(△H1+△H2+3△H3) | B. | △H4=$\frac{2}{3}$(3△H3-△H1-△H2) | ||
| C. | △H4=$\frac{2}{3}$ (△H1+△H2-3△H3) | D. | △H4=$\frac{3}{2}$(△H1-△H2-3△H3) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
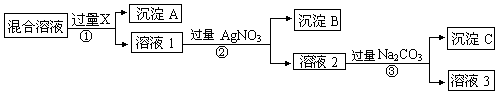
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
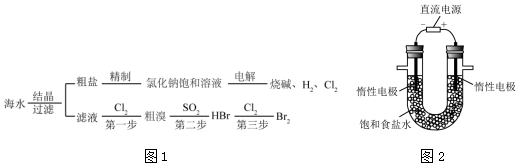
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com