
已知X为第三周期元素的原子,该原子要达到8 电子稳定结构,则需要的电子数小于其 次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是 ( )
电子稳定结构,则需要的电子数小于其 次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是 ( )
A.X元素最高价氧化物对应的水化物一定是强酸
B.X元素的氢化物的化学式一定为H2X
C.X的单质一定是良好的半导体材料
D.X元素的氧化物一定能与烧碱反应
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
硝酸铜是一种重要的工业产品,化学上有很多方法可以制取硝酸铜:①将铜溶于硝酸中、②先将铜与O2反应生成CuO,再溶于硝酸中、③将铜溶于N2O4的乙酸乙酯(溶剂,不参加反应)溶液中生成硝酸铜和一氧化氮。下列认识或判断错误的是 ( )。
A.方法③是最经济和环保的
B.方法①中,若从经济和环保的角度考虑,用稀硝酸比用浓硝酸好C.方法②需要消耗能源,对环境不产生污染
D.方法③中N2O4既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验,从实验可以判断:

A.该固体粉末中一定不含有BaCl2
B.该固体粉末中一定含有KNO3
C.它的组成可能是CaCO3、BaCl2、CuSO4
D.它的组成一定是CaCO3、Na2SO4、KNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
化学键使得一百多种元素构成了世界的万物。关于化学键的下列叙述中,正确的是( )。
A.离子化合物中一定含有共价键,共价化合物中不含离子键
B.共价化合物中可能含离子键,离子化合物中只含离子键
C.构成单质分子的粒子一定含有 共价键
共价键
D.在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、
原子核与原子核之间的排斥作用
查看答案和解析>>
科目:高中化学 来源: 题型:
下面所 列的是一组你熟悉的物质:
列的是一组你熟悉的物质:
①HCl ②CO2 ③H2O ④H2 ⑤NaOH ⑥Cl2
⑦NaF ⑧CH4 ⑨CaO ⑩MgCl2
(1)只含有共价键的是___ _____,只含有离子键的是________,既含离子键,又含有共价键的是________。
_____,只含有离子键的是________,既含离子键,又含有共价键的是________。
(2)属于共价化合物的是________,属于离子化合物的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是  ( )。
( )。
A.两种微粒,若核外电子排布完 全相同,则其化学性质一定相同
全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子如果核外电子排布相同,则一定属于同种元 素D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
素D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子能够大量共存的是 ( ) A.Mg2+、K+、SO42-、NO3- B.Ba2+、Mg2+、SO42+、Cl-
C.ClO-、K+、Na+、H+ D.H+、K+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种可溶性盐,它们分别是AgNO3、CuSO4、Na2CO3、BaCl2中的一种,现进行如下实验:
①、若把四种盐分别溶解于盛有蒸馏水的四个试管中,只有C的溶液呈蓝色
②、若把①中的四支试管中分别加入盐酸,B的溶液由沉淀生成,D的溶液有无色无味的气体逸出。
(1)写出下列物质的化学式:
A.______________B.______________C.______________D.______________
(2)写出实验②中有关反应的离子方程式:
_________________________________________________________________。
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O2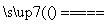 2O3
2O3
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气体的平均摩尔质量为________g/mol(保留一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为________L。
(3)实验 室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热
室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热 后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为________。
后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com