
某无色溶液中含有K+,Cl-,OH-,SO32-,SO42-,为了检验除OH-外的其它所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氢氧化钡溶液、溴水和酚酞六种试剂,设计如下实验步骤,并记录相关现象: 下列有关结论错误的是 ( )
下列有关结论错误的是 ( )
| A.试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl |
| B.现象3中白色沉淀是BaSO4 |
| C.试剂②是盐酸,试剂③是硝酸 |
| D.产生现象2的离子方程式是:Br2+2H2O+SO2=4H++2Br-+SO42- |
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:单选题
能正确表示下列反应的离子方程式是:
| A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| B.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ |
| C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ |
| D.向FeCl3溶液中加入Mg(OH)2: 3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )。
| A.Fe3+、K+、Cl-、NO3- | B.Ag+、Na+、NO3-、Cl- |
| C.Zn2+、Al3+、SO42-、Cl- | D.Ba2+、NH4+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应的离子方程式书写正确的是( )
| A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| B.稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀 H2SO4反应:Ba2++SO42-=BaSO4↓ |
| D.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在无色透明的酸性溶液中,能大量共存的离子组是( )
| A.Na+、Ag+、S2-、SO42- | B.Mg2+、NH4+、NO3- 、Cl- |
| C.Na+、K + 、SO32-、CH3COO- | D.Cu2+、Na+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某无色待测液中可能含有 、
、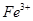 、
、 、
、 、
、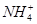 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:
I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入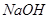 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
请回答下列问题:
(1)待测液中一定含有的离子是__________,一定不含有的离子是___________。
(2)还有一种离子不能确定是否存在,检验这种离子的实验方法是__________,观察到的现象是_______________________。
(3)请你写出“步骤III”中产生气体的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式书写正确的是
| A.钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| B.硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+===BaSO4↓ |
| C.碳酸钙与醋酸反应:CaCO3+2H+===Ca2++CO2↑+H2O |
| D.NaOH溶液中通入少量SO2:2OH-+SO2 ══ SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子一定能大量共存的是( )
| A.滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- |
| B.C(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br- |
| C.CO32-可以大量共存的溶液:Na+、K+、NO3-、Al3+ |
| D.由水电离的c(H+)=1.0×10-13 mol·L-1的溶液中:K+、NH4+、AlO2-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com