
| A. | 1 | B. | 2 | C. | 3 | D. | 6 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 、④HCHO等,其中碳原子不是采取sp2杂化的分子有②(填物质编号),HCHO分子的立体构型为平面三角形.
、④HCHO等,其中碳原子不是采取sp2杂化的分子有②(填物质编号),HCHO分子的立体构型为平面三角形.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
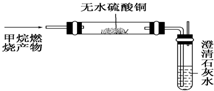 (1)我国西周年代写成的算卦占卜的书《周易》中,在谈到一些自然界发生的现象时说:“象曰:‘泽中有火’”试用化学方程式表示出泽中有火的化学反应CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O.西气东输是我国油气管道建设史上距离最长的输气管道,总长3900公里,设计年输气量120亿立方米.这里说的气就是天然气,天然气的主要成分是甲烷(填名称),试分析使用天然气的优点清洁无污染.
(1)我国西周年代写成的算卦占卜的书《周易》中,在谈到一些自然界发生的现象时说:“象曰:‘泽中有火’”试用化学方程式表示出泽中有火的化学反应CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O.西气东输是我国油气管道建设史上距离最长的输气管道,总长3900公里,设计年输气量120亿立方米.这里说的气就是天然气,天然气的主要成分是甲烷(填名称),试分析使用天然气的优点清洁无污染.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
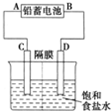 如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极).
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钢板是正极,正极上发生还原反应 | |
| B. | 放电时电子的流向:正极→导线→负极 | |
| C. | 放电时OH-向正极移动 | |
| D. | 放电时总反应为:4Li+2H2O+O2=4LiOH |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
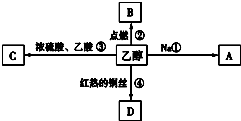 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳的化合物.
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳的化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com