
【题目】下表列出了①~⑥六种元素在元素周期表中的位置。
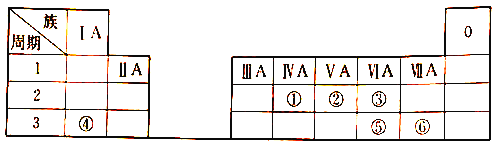
请回答下列问题:
(1) ①元素原子的质子数是_________。
(2)②元素的最简单氢化物的分子式是_______。
(3)③和⑤两种元素的非金属性: ③___⑤(填“>”“<”或“=”);
(4)④和⑥两种元素的最高价氧化物对应的水化物相互反应的离子方程式为_______。
科目:高中化学 来源: 题型:
【题目】用图装置(气密性好)研究钠与氯气的反应。

实验步骤:
①将一定量浓盐酸滴在KMnO4粉末上,立即产生黄绿色气体。
②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
(1)步骤①,黄绿色气体是氯气,则KMnO4的作用是__________(填“氧化剂”或“还原剂”)。
(2)步骤③,引起钠燃烧的原因是____________。
(3)生成白色固体的化学方程式是______________。
(4)结合离子方程式说明NaOH溶液的作用是_______________。
(5)实验结束后,甲同学在安全、环保的理念指导下,仅用上图装置就完成了集气瓶内残余氯气的处理,其操作是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种优良的消毒剂,熔点为-59℃,沸点为 11℃,浓度过高时易发生分解,甚至爆炸。某课外兴趣小组通过氯气与 NaClO2溶液反应来制取少量ClO2,装置如下图所示:
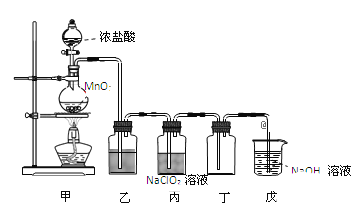
(1)甲装置中圆底烧瓶内发生反应的化学方程式是_________________________________________。
(2)丙装置中发生的反应可能经两步完成,请将其补充完整:
①____________________________________________(用化学方程式表示),
②HClO + HCl + 2NaClO2 2ClO2↑+ 2NaCl + H2O。
(3)Clˉ存在时会催化 ClO2的生成,若无乙装置,则丙装置内产生 ClO2的速率明显加快。乙装置中试剂瓶内的液体是__________。戊装置的作用是_______________________。
(4)戊装置烧杯中 NaOH 溶液吸收 ClO2后,生成了 ClO![]() 、ClO
、ClO![]() ,该反应的离子方程式是_______________________________________。
,该反应的离子方程式是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:

回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2的作用是____________。写出操作①的名称:________。
(2)反应Ⅱ是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式:__________________________________________。操作②用到的主要仪器名称为______________,其目的是(填序号)________。
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加Cu2+在水中的溶解度
(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和________。若操作③使用如图装置,图中存在的错误是__________________________________________。

(4)操作④以石墨作电极电解CuSO4溶液。阴极析出铜,阳极产物是________________。 流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝和铁是日常生活中两种常见的金属,铝和铁的化合物是中学化学中常见的基础物质。请回答下列有关问题:
(1)氧化铝是一种_____氧化物(填“酸性”“碱性”或“两性”);
(2)实验室制备氢氧化铝时,最好向铝盐溶液中加入_____。(填“氨水”或“氢氧化钠溶液”);
(3)还原铁粉与水蒸气反应的化学方程式为3Fe+4H2O(g) ![]() X+4H2,试推测X的化学式为_____。
X+4H2,试推测X的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,4二氯苯乙酸是生产新型杀虫、杀螨剂螺螨酯的关键中间体,其结构简式如图所示。下列有关说法错误的是( )

A. 该有机物能发生加成反应、取代反应
B. 该有机物的分子式为C8H6Cl2O2
C. 改变氯原子在苯环上的位置,还可得到8种结构
D. 该有机物分子中所有的碳原子可能同时处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 100 g 质量分数为46%的乙醇(CH3CH2OH)水溶液中氧原子数为4NA
B. 标况下,46g NO2所含分子数目为NA
C. 1 mol Cl2通入足量NaOH溶液中,转移电子数为2NA
D. 0.5mol/L 的H2SO4溶液中,含有H+的个数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组采用刻蚀废液(主要含CuCl2、FeCl3、FeCl2、HCl)制取Cu和Cu2Cl2,实验流程如下:

已知:Cu2Cl2是白色固体,微溶于水,难溶于乙醇,受潮后在空气中易被迅速氧化。
(1)“预处理”时,需用Na2CO3调节溶液至微酸性而不是碱性,其原因是__________________。
(2)“还原Ⅰ”需在80 ℃条件下进行,适宜的加热方式为____________。
(3)“还原Ⅱ”中,Cu2+参与反应的离子方程式为__________________。
(4)“搅拌”时加入NaCl粉末的作用是____________________________。
(5)“过滤Ⅱ”得到的Cu2Cl2需用无水乙醇洗涤,并在真空干燥机内于70 ℃干燥2小时,冷却,密封包装。于70 ℃真空干燥的目的是__________________________。
(6)①设计从“过滤Ⅰ”所得滤渣中获取Cu的实验方案:稀硫酸加到滤渣中,搅拌,充分反应至无气体产生为止,过滤并用蒸馏水洗涤2~3次,低温烘干。
②现欲测定途径a、b回收铜元素的回收率比,请补充实验方案:____________________,分别按途径a、b制取Cu和Cu2Cl2,测得Cu的质量为m1 g,Cu2Cl2的质量为m2 g,则途径a、b铜元素的回收率比为________(铜元素回收率=产品中铜元素质量/废液中铜元素的质量×100%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡时,各物质的物质的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持温度不变,以2∶2∶1的物质的量之比再充入A,B,C,则( )
2C(g)达到平衡时,各物质的物质的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持温度不变,以2∶2∶1的物质的量之比再充入A,B,C,则( )
A. 平衡向正方向移动 B. 平衡不发生移动
C. C的体积分数减小 D. C的体积分数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com