
| A. | 次氯酸的结构式:H-Cl-O | B. | CO2的比例模型 | ||
| C. | NH4Cl的电子式: | D. | 苯乙烯的结构简式: |
分析 A.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合;
B.比例模型表示原子的相对大小及原子连接顺序、空间结构;
C.氯离子为阴离子,电子式中需要标出其最外层电子;
D.苯乙烯可以看作苯基取代了乙烯分子中的1个H形成的,据此写出其结构简式.
解答 解:A.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合,结构式为H-O-Cl,故A错误;
B.二氧化碳的分子式为CO2,二氧化碳为直线型结构,其比例模型中碳原子的相对体积大于氧原子,二氧化碳正确的比例模型为 ,故B错误;
,故B错误;
C.氯化铵属于离子化合物,铵根离子和氯离子都需要标出所带电荷及最外层电子,氯化铵正确的电子式为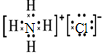 ,故C错误;
,故C错误;
D.苯乙烯分子中含有1个苯环和1个碳碳双键,其结构简式为 ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及结构简式、电子书、比例模型等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题的能力.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器气体密度不随时间变化 | |
| B. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| C. | 容器内各物质的浓度不随时间变化 | |
| D. | 单位时间消耗0.1 mol X同时生成0.2 mol Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸 | B. | 烧碱溶液 | C. | 氨水 | D. | KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LSO3含有NA个分子 | |
| B. | 6.4g氧气和3.2g臭氧(O3)混合气体所含有的氧原子数为0.6NA | |
| C. | 过氧化钠与CO2反应时,0.1mol过氧化钠转移的电子数为0.2NA | |
| D. | 标准状况下,2.24L Cl2与过量的稀FeCl2溶液反应,转移电子总数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水 | B. | 溴水 | C. | 稀硫酸 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸中:K+、Mg2+、AlO2-、NO3- | |
| B. | Na2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | $\frac{Kw}{c({H}^{+})}$=10-13 mol•L-1溶液中:Fe3+、NH4+、Mg2+、SO42- | |
| D. | 通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com