
【题目】下列指定反应的离子方程式正确的是
A.将铜丝插入稀硝酸中:Cu+4H++2![]() =Cu2++2NO2↑+2H2O
=Cu2++2NO2↑+2H2O
B.漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.硫酸铜溶液与过量的氨水反应:Cu2++4NH3H2O=[Cu(NH3)4]2++4H2O
D.用惰性电极电解MgCl2溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
【答案】C
【解析】
A.Cu与稀硝酸反应生成NO而不是NO2,该离子方程式不符合客观事实,正确的离子方程式为:3Cu+8H++2![]() =3Cu2++2NO↑+4H2O,A项错误;
=3Cu2++2NO↑+4H2O,A项错误;
B.漂白粉溶液中通入少量SO2,ClO-具有强氧化性,会将![]() 氧化为
氧化为![]() ,正确的离子方程式为:Ca2++3ClO-+SO2+H2O=CaSO4↓+2HClO+Cl-,B项错误;
,正确的离子方程式为:Ca2++3ClO-+SO2+H2O=CaSO4↓+2HClO+Cl-,B项错误;
C.硫酸铜溶液与过量的氨水反应生成铜氨络合物,离子方程式为:Cu2++4NH3H2O=[Cu(NH3)4]2++4H2O,C项正确;
D.用惰性电极电解MgCl2溶液,根据阴阳离子放电顺序可知生成了H2、Cl2和Mg(OH)2,Mg(OH)2为沉淀,不能拆分,正确的离子方程式为:Mg2++2Cl-+2H2O![]() H2↑+Cl2↑+Mg(OH)2↓,D项错误;
H2↑+Cl2↑+Mg(OH)2↓,D项错误;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】磷烯(如图)是由磷原子六元环组成的蜂巢状褶皱二维晶体,它是白磷(![]() )的同素异形体。设NA为阿伏加德罗常数,下列说法正确的是
)的同素异形体。设NA为阿伏加德罗常数,下列说法正确的是
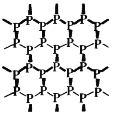
A.3.1g白磷中含P—P键的数目为0.3NA
B.6.2g磷烯中含六元环的数目为0.1NA
C.0.1molP4与0.6molH2在密闭容器中发生反应P4+6H2![]() 4PH3,生成PH3分子的数目为0.4NA
4PH3,生成PH3分子的数目为0.4NA
D.0.1molP4发生反应P4+5O2=2P2O5,转移的电子数为20NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中①到⑩10种元素,填写下表空白:

(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是______,碱性最强的化合物的化学式是______。![]() 均填化学式
均填化学式![]()
(2)最高价氧化物对应的水化物是两性的元素是______![]() 填元素符号
填元素符号![]() ,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式______。
,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式______。
(3)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是![]() 用离子符号表示
用离子符号表示![]() ______。
______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、用![]() 表示原子,N表示中子数。
表示原子,N表示中子数。
⑴阳离子的中子数:![]() 共有x个电子,则
共有x个电子,则![]() _______。
_______。
⑵阴离子的中子数:![]() 共有x个电子,则
共有x个电子,则![]() ________。
________。
⑶A2-原子核内有x个中子,其质量数为m,则ng A2-所含电子的物质的量为______mol。
Ⅱ、下列变化:
①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氯气溶于水⑥氯化铵受热分解。
⑷未发生化学键破坏的是________;![]() 填序号,下同
填序号,下同![]() 仅发生离子键破坏的是__________。
仅发生离子键破坏的是__________。
⑸若上述物质都为纯净物时,属于共价化合物的是_____;属于离子化合物的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。下列说法错误的是
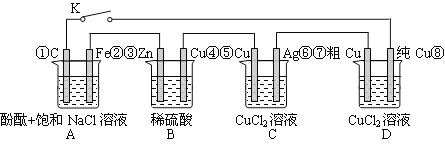
A.当K闭合时,A装置发生吸氧腐蚀,在电路中做电源
B.当K断开时,B装置锌片溶解,有氢气产生
C.当K闭合后,整个电路中电子的流动方向为①→⑧;⑦→⑥;⑤→④;③→②
D.当K闭合后,A、B装置中pH变大,C、D装置中pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g)。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。下列说法正确的是
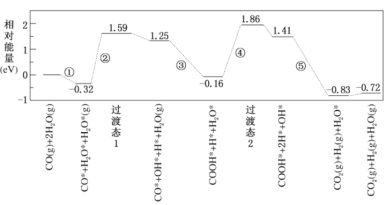
A.水煤气变换反应的△H>0
B.步骤③的化学方程式:CO*+OH*+H2O(g)=COOH*+H2O*
C.步骤⑤只有非极性键HH键形成
D.该历程中最大能垒(活化能)E正=1.70eV
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下一些氧化物和单质之间可发生如下图所示的反应:其中,氧化物Ⅰ是红棕色固体,氧化物Ⅱ、Ⅲ、Ⅳ在反应条件下都是气体。
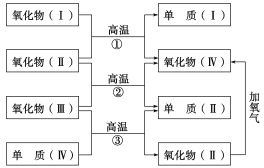
(1)氧化物Ⅰ的化学式是________,氧化物Ⅱ的化学式是________。
(2)反应①的化学方程式是_________;反应②的化学方程式_______;反应③的化学方程式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将 1.0 L w mol·L-1 CH3COOH 溶液与 0.1 mol NaOH固体混合,充分反应。然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),溶液pH的变化如图。下列叙述正确的是
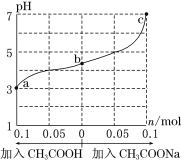
A.b点混合液中c(Na+)>c(CH3COO-)
B.加入CH3COOH过程中,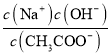 增大
增大
C.c点存在:c(CH3COOH)+c(CH3COO-) =0.1+w
D.a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体[CH3CH(OH)COO]2Fe·3H2O(M=288 g/mol)是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸CH3CH(OH)COOH与FeCO3反应制得.
I.制备碳酸亚铁
(1)利用如图所示装置进行实验。装置中仪器C的名称是____________。

(2)实验开始时,首先关闭活塞2,打开活塞1、3,目的是________________________;关闭活塞1,反应一段时间后,关闭活塞_________,打开活塞___________,观察到B中溶液进入到C中,C中产生沉淀和气体。生成FeCO3的离子方程式为__________。
(3)装置D的作用是___________________。
Ⅱ.乳酸亚铁晶体的制备及纯度测定
将制得的FeCO3加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸,从所得溶液中获得乳酸亚铁晶体。
(4)加入少量铁粉的作用是______________________________。
(5)用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其主要原因是____________________________________________。
(6)经查阅文献后,改用Ce(SO4)2标准溶液进行滴定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.760 g样品,溶解后进行必要处理,用容量瓶配制成250 mL溶液,每次取25.00 mL,用0.1000 mol·L-1Ce(SO4)2标准溶液滴定至终点,记录数据如下表所示:

则产品中乳酸亚铁晶体的纯度为________%(保留小数点后两位)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com