
���� ��1������CO2+2NaOH�TNa2CO3+H2O��CO2+NaOH�TNaHCO3��������
��2�����ݷ�Ӧ������̼���ƣ�������̼����������д���ӷ�Ӧ����ʽ��
��3����ɫ����Ϊ̼��ƣ�����̼ԭ���غ�ɼ��������̼��������
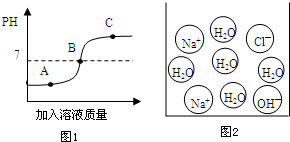
��� �⣺��1���ٵ�CO2��NaOH�����ʵ�����С��1��2ʱ���ɷ�ӦCO2+2NaOH�TNa2CO3+H2O��֪��Ӧ����̼���ƣ�����ʣ���NaOH����ѹ���µ�������������Һ���õ���ɫ����ΪNaOH��Na2CO3 ��
�ڵ�������̼��NaOH�����ʵ���Ϊ1��2ʱ����ӦCO2+2NaOH�TNa2CO3+H2Oǡ����ȫ���У�����Һ�е�����ΪNa2CO3����ѹ���µ�������������Һ���õ���ɫ����ΪNa2CO3 ��
�۵�������̼��NaOH�����ʵ����ȴ���1��2����С��1��1ʱ������CO2+2NaOH�TNa2CO3+H2O��CO2+NaOH�TNaHCO3����ѹ���µ�������������Һ���õ���ɫ����ΪNa2CO3��NaHCO3 ��
�ܵ�������̼��NaOH�����ʵ����ȡ�1��1ʱ������CO2+NaOH�TNaHCO3����ѹ���µ�������������Һ���õ���ɫ����Ϊ
NaHCO3��
�ʴ�Ϊ��NaOH��Na2CO3 ��Na2CO3��Na2CO3��NaHCO3 ��NaHCO3��
��2����CO2����ͨ��NaOH��Һ�У��ȷ���CO2+2NaOH�TNa2CO3+H2O������Na2CO3+H2O+CO2�TNaHCO3�����ӷ�Ӧ�ֱ�ΪCO2+2OH-=CO32-+H2O��CO32-+H2O+CO2=2HCO3-��
�ʴ�Ϊ��CO2+2OH-=CO32-+H2O��CO32-+H2O+CO2=2HCO3-��
��3�����ɫ����Ϊ̼��ƣ���̼ԭ���غ��֪��������̼������Ϊ$\frac{ag}{100g/mol}$��44g/mol=$\frac{11}{25}$ag���ʴ�Ϊ���ܣ�$\frac{11}{25}$ag��
���� ���⿼���йع�������ļ��㣬Ϊ��Ƶ���㣬��ȷ�����Ļ�ѧ��Ӧ����ѧ�����ü��˼��衢ԭ���غ�������ǽ����Ĺؼ�����Ŀ�ѶȲ���


 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2CH3CH2OH $��_{140��}^{ŨH_{2}SO_{4}}$ CH3CH2OCH2CH3+H2O | |
| B�� | CH3COOC2H5+H2O $��_{��}^{ϡH_{2}SO_{4}}$ CH3COOH+C2H5OH | |
| C�� | 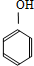 +3Br2�� +3Br2��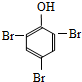 +3HBr +3HBr | |
| D�� | 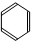 +CH2=CH2$��_{��}^{����}$ +CH2=CH2$��_{��}^{����}$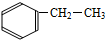 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��28g����ϩ��֬�У����е�̼ԭ�Ӹ���Ϊ2NA | |
| B�� | ���������֮�Ͳ�һ�����������ɵĸ߾�������� | |
| C�� | ���۷�Ӧ�ĵ����������������� | |
| D�� | ����ͨ����˵������ϳɲ�����ָ���ϡ��ϳ����ϳ���ά |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Һ����Ĺ���ʵ���Ͼ��ǵ��Ĺ��� | |
| B�� | ���õ�ⱥ��ʳ��ˮ���õIJ�������������� | |
| C�� | ����ȼ�ϵ�صĸ���ͨ��������� | |
| D�� | ͭ�����Ի������������ⸯʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ֱ����1��100nm֮�� | B�� | �����������˶� | ||
| C�� | ����ͨ��������������� | D�� | ������������Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ƿ����Ͳ�͵ζ����϶�����ʹ���¶ȣ���Ͳ������ƿ�ޡ�0���̶ȣ��ζ����С�0���̶ȣ�ʹ��ʱ�ζ���ˮϴ������ϴ��������ƿˮϴ������ϴ | |
| B�� | �õ�����ƽ������ѧҩƷʱ�������ȳ�С�ձ����������ٳ��������Լ����������������֮�ΪҩƷ������ | |
| C�� | �����Ż�ʱ������ϸɳ������𣻵����豸����Ļ��֣�������ĭ�������� | |
| D�� | �ڷ�̪��Һ�м���������Ʒ�ĩ����Һ��ɫ���ȱ�����ɫ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
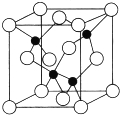 X��Y��Z��U��W��ԭ���������������ǰ������Ԫ�أ�����Y��ԭ�Ӻ�����7���˶�״̬��ͬ�ĵ��ӣ�X��Z��δ�ɶԵ�������Ϊ2��U�ǵ�������Ԫ���γɵļ������а뾶��С��Ԫ�أ�W���ڲ����ȫ�����������ֻ��1�����ӣ���ش��������⣺
X��Y��Z��U��W��ԭ���������������ǰ������Ԫ�أ�����Y��ԭ�Ӻ�����7���˶�״̬��ͬ�ĵ��ӣ�X��Z��δ�ɶԵ�������Ϊ2��U�ǵ�������Ԫ���γɵļ������а뾶��С��Ԫ�أ�W���ڲ����ȫ�����������ֻ��1�����ӣ���ش��������⣺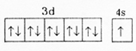 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
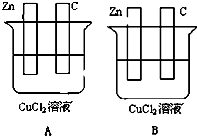 ��ͼ��ʾ��A��B���ձ��о�ΪCuCl2��Һ�����������Ա�Ҫ�����Ӳ���գ�
��ͼ��ʾ��A��B���ձ��о�ΪCuCl2��Һ�����������Ա�Ҫ�����Ӳ���գ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com