
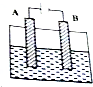
 根据下列装置图,回答问题.
根据下列装置图,回答问题.分析 (1)电解氯化镁溶液,阳极生成氯气,阴极生成氢气和氢氧化镁沉淀;
(2)若A为Cu,B为碳棒,电解质溶液为CuSO4溶液,为电镀铜装置;
(3)若A为碳棒,B为铁,电解质为熔融NaCl,阳极生成氯气,阴极生成钠.
解答 解:(1)电解氯化镁溶液,阳极生成氯气,阴极生成氢气和氢氧化镁沉淀,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H2O+2e-+Mg2+=Mg(OH)2↓+H2↑,总反应式为Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+Mg(OH)2↓,
故答案为:2Cl--2e-=Cl2↑;2H2O+2e-+Mg2+=Ma(OH)2↓+H2↑;Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+Mg(OH)2↓;
(2)若A为Cu,B为碳棒,电解质溶液为CuSO4溶液,为电镀铜装置,阳极反应为Cu-2e-=Cu2+,阴极反应为Cu2++2e-=Cu,
故答案为:Cu-2e-=Cu2+;Cu2++2e-=Cu;
(3)若A为碳棒,B为铁,电解质为熔融NaCl,阳极生成氯气,电极方程式为2Cl--2e-=Cl2↑,阴极生成钠,电极放出为Na++e-=Na,总方程式为2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑,
故答案为:2Cl--2e-=Cl2↑;Na++e-=Na;2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑.
点评 本题考查了电解池原理,能正确判断电解池的阴阳极是解本题的关键,注意把握阴阳极上离子的放电顺序,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ③>①>④>② | B. | ①>②>③>④ | C. | ③>②>①>④ | D. | ①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | K1闭合,铁棒上发生的反应为2H++2e-═H2↑ | |
| B. | K1闭合,石墨棒周围溶液pH逐渐降低 | |
| C. | K2闭合,铁棒不易被腐蚀,电路中通过0.001NA个电子时,摇匀后溶液的pH为11 | |
| D. | K2闭合,电路中通过0.002 NA个电子时,两极共产生0.002mol气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在烧烤过程中,肉类中的蛋白质在高温下发生变性 | |
| B. | 有部分烧烤摊使用了地沟油,地沟油经过精炼后可以食用 | |
| C. | 为了食品卫生,鼓励烧烤摊大量使用一次性竹签 | |
| D. | 露天烧烤产生的大量PM2.5能在空气中形成胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下两种气体的体积之比等于物质的量之比 | |
| B. | 同温同压下两种气体的物质的量之比等于密度之比 | |
| C. | 同温同压下两种气体的摩尔质量之比等于密度之比 | |
| D. | 同温同体积下两种气体的物质的量之比等于压强之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L SO3中原子数目为4NA | |
| B. | 100mL 1mol•L-1的K2CO3溶液中CO32-数目为0.1NA | |
| C. | 5.6g N2与足量H2反应,转移电子数目小于1.2NA | |
| D. | 9.1g苯和立方烷(C8H8)的混合物中原子数目为0.7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、一氯甲烷、二氯甲烷等均属于烷烃 | |
| B. | 乙醇不与任何酸反应 | |
| C. | 乙酸不能与金属Na反应 | |
| D. | 乙酸乙酯能发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com