
| A. | 9:4 | B. | 4:9 | C. | 2:1 | D. | 1:2 |
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作与现象 | 结论 |
| A | 向鸡蛋清溶液中滴加醋酸铅溶液,产生白色沉淀,加水沉淀不消失 | 蛋白质发生了变性 |
| B | 测定浓度均为0.1mol•L-1 CH3COONa与HCOONa溶液的pH,CH3COONa溶液的pH较大 | 酸性:CH3COOH>HCOOH |
| C | 苯酚的浊液中加入碳酸钠溶液,溶液变为无色 | 酸性:苯酚>碳酸氢钠溶液 |
| D | 向浓度均为0.1mol•L-1 NaCl和NaI混合溶液中滴加3滴0.1mol•L-1 AgNO3溶液,出现黄色沉淀 | 溶解度:AgI<AgCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H2O═4NaOH+O2↑是水作还原剂的氧化还原反应 | |
| B. | 1mol Na2O2固体中含离子总数为4NA | |
| C. | 用灼烧的方法除去Na2CO3中的NaHCO3 | |
| D. | NaHCO3溶液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液在电流作用下电离成Na+和Cl- | |
| B. | 溶于水后能够电离出H+的化合物都是酸 | |
| C. | 氯化氢溶于水形成的溶液能够导电,所以氯化氢是电解质 | |
| D. | CO2溶于水形成的溶液能够导电,所以CO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | 两试管各加入5ml 0.1mol/L Na2S2O3溶液,同时分别滴入5ml 0.1mol/L硫酸和盐酸 | 两支试管同时变浑浊 | 其它条件不变时,Cl-一定有催化效果 |
| C | A1箔插入稀HNO3中 | 无现象 | A1箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每消耗1molCH4可以向外电路提供4mole- | |
| B. | 在负极上O2获得电子,电极反应式为 O2+2H2O+4e-=4OH- | |
| C. | 外电路电子由负极流向正极,内电路电子由正极流向负极 | |
| D. | 电池放电过程中,溶液的PH不断降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中加稀盐酸入:HCO3-+H+═CO2↑+H2O | |
| B. | 碳酸钡和稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 铜片插入硝酸银溶液:Cu+Ag+═Cu2++Ag | |
| D. | 把金属铁放入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2的电子式: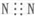 | |
| B. | S2-的结构示意图: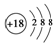 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{58}^{131}$I | |
| D. | 乙烯的分子式:CH2=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol•L-1 | |
| B. | 常温常压下,5.6g乙烯与丁烯(C4H8)的混合物中氢原子数为0.8NA | |
| C. | 标准状况下,4.48 LCl2与足量的Fe反应转移电子数为0.4NA | |
| D. | 0.1 mol H218O与D2O的混合物中中子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com