
����Ŀ�������ҹ����Ԫ�أ����۵���ߵĽ������㷺�������Ƶ��ݵĵ�˿�� ��������ʹ������������������Ȼ����Ҫ���� (+6��) ���ε���ʽ���ڡ��п��ɼ�ֵ���ٿ�ʯ�ǰ��ٿ�ͺ��ٿ��ٿ����Ҫ�ɷ�������ƣ�CaWO4�������ٿ����Ҫ�ɷ��������̵������Σ���ѧʽ��д��(FeWO4��MnWO4)�����ᣨH2WO4�����Ժ�����������ˮ��
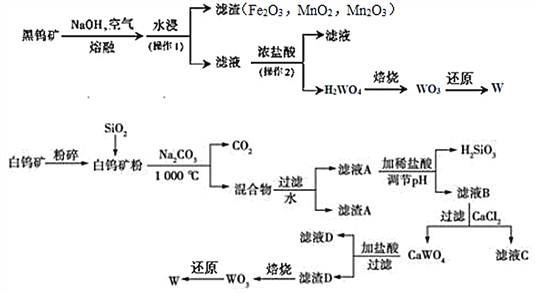
��֪����CaWO4��̼���ƹ��ȷ������ֽⷴӦ��
�����ڸ����¿��뽹̿(C)��Ӧ����Ӳ�ʺϽ�̼����(WC)��
��1��74W�����ڱ���λ���ǵ�_______���ڡ�
��2��д�����ٿ���FeWO4���������ƣ���������ʱ�Ļ�ѧ��Ӧ����ʽ________________________________�����ٿ����̼���ƹ��ȵĻ�ѧ��Ӧ����ʽ_______________��
��3����ҵ�ϣ�����һ����̼������������ԭWO3ұ��W�������ϣ������ʵ�����CO��H2��Al����ԭ�����ɵõ�W������֮��Ϊ______���ý�̿Ҳ�ܻ�ԭWO3�����������������ŵ㣬��������_____________________________________��
��4����֪�������ƺ������(CaWO4)�����ܵ���ʣ����ߵ��ܽ�Ⱦ����¶����߶���С����ͼΪ��ͬ�¶���Ca(OH)2��CaWO4�ij����ܽ�ƽ�����ߣ���T1ʱKsp(CaWO4)��_________(mol/L)2������������Һ����ʯ����õ���������ƣ�������Ӧ�����ӷ���ʽΪ_____________________________��T2ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ__________��

��5����ҵ�ϣ����õ�ⷨ��̼���ٷ����л����١�̼�����������������������������Ϊ�������Һ��������������D���ų�CO2��д�������ĵ缫��Ӧʽ_______________��
���𰸡� �� 4 FeWO4+8NaOH+O2![]() 2Fe2O3+4Na2WO4+4H2O CaWO4+Na2CO3
2Fe2O3+4Na2WO4+4H2O CaWO4+Na2CO3![]() CaCO3+Na2WO4 2��2��3 ��̿Ϊ���壬�õ��Ľ����ٻ���й������ʣ������ý�̿�����ܲ���CO������Ⱦ��β�� 1��10-10 WO42-+ Ca(OH)2=CaWO4+ 2OH- 1��103 mol/L WC��10e-+6H2O= H2WO4+CO2+ 10H+
CaCO3+Na2WO4 2��2��3 ��̿Ϊ���壬�õ��Ľ����ٻ���й������ʣ������ý�̿�����ܲ���CO������Ⱦ��β�� 1��10-10 WO42-+ Ca(OH)2=CaWO4+ 2OH- 1��103 mol/L WC��10e-+6H2O= H2WO4+CO2+ 10H+
��������(1)WΪ74��Ԫ�أ������������һ��Ԫ��Ϊ56�ţ������������һ��Ԫ��Ϊ84�ţ����74����Ԫ�����ڱ��ĵ������ڣ��ʴ�Ϊ������
(2)FeWO4�е���Ϊ+2�ۣ������������ڿ�������ʱ�������е�������������Ӧ�Ļ�ѧ��Ӧ����ʽΪ4 FeWO4+8NaOH+O2![]() 2Fe2O3+4Na2WO4+4H2O�����ٿ����̼���ƹ��ȵĻ�ѧ��Ӧ����ʽΪCaWO4+Na2CO3
2Fe2O3+4Na2WO4+4H2O�����ٿ����̼���ƹ��ȵĻ�ѧ��Ӧ����ʽΪCaWO4+Na2CO3![]() CaCO3+Na2WO4���ʴ�Ϊ��4 FeWO4+8NaOH+O2
CaCO3+Na2WO4���ʴ�Ϊ��4 FeWO4+8NaOH+O2![]() 2Fe2O3+4Na2WO4+4H2O��CaWO4+Na2CO3
2Fe2O3+4Na2WO4+4H2O��CaWO4+Na2CO3![]() CaCO3+Na2WO4��
CaCO3+Na2WO4��
(3)��ҵ�ϣ�����һ����̼������������ԭWO3ұ��W�������ϣ�1mol��CO��H2��Al����ԭ��ʱ��ת�Ƶĵ��ӷֱ�Ϊ2mol��2mol��3mol�����ݵ�ʧ�����غ㣬�õ�W������֮��Ϊ2��2��3���ý�̿Ҳ�ܻ�ԭWO3�����������������ŵ㣬��Ϊ��̿Ϊ���壬�õ��Ľ����ٻ���й������ʣ������ý�̿�����ܲ���CO������Ⱦ��β�����ʴ�Ϊ��2��2��3����̿Ϊ���壬�õ��Ľ����ٻ���й������ʣ������ý�̿�����ܲ���CO������Ⱦ��β����
(4)����ͼ��T1ʱKSP(CaWO4)=c(Ca2+)c(WO42-)=1��10-5��1��10-5=1��10-10������������Һ����ʯ���飬�������ֽⷴӦ���������ƺ���������ӷ�Ӧ��������Ƴ�������Ӧ�����ӷ���ʽΪ��WO42-+Ca(OH)2=CaWO4+2OH-��T2ʱ��C(OH-)=10-2mol/L��c(WO42-)=10-7mol/L��ƽ�ⳣ��K����������ƽ��Ũ��ϵ���η�֮���ͷ�Ӧ��ƽ��Ũ��ϵ���η�֮������K=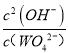 =
=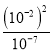 =1��103���ʴ�Ϊ��1��10-10��WO42-+Ca(OH)2=CaWO4+2OH-��1��103��
=1��103���ʴ�Ϊ��1��10-10��WO42-+Ca(OH)2=CaWO4+2OH-��1��103��
(5)���ʱ�������������ӷŵ������������缫��Ӧʽ��2H++2e-=H2����������̼����ʧȥ���ӣ�����������Ӧ��WC+6H2O-10e-=H2WO4+CO2��+10H+���ʴ�Ϊ��WC+6H2O-10e-=H2WO4+CO2��+10H+��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���![]() ��ҽҩ�ϳ������Ź㷺����;�����ж��ظ����ʵ�˵����ȷ����
��ҽҩ�ϳ������Ź㷺����;�����ж��ظ����ʵ�˵����ȷ����
A. �û������к���������Ϊ����
B. �û�̨���е�����̼ԭ��һ������ͬһƽ����
C. �û�����ɷ���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ
D. �û������ͬ���칹���У�������������ȡ�����Ĺ�3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӣ�N2��CO2��NH3��N2O��NO2��NO2����NO��CO��
(1)��Ϊ�ȵ������������________________��
(2)����Mg������N2O��ȼ�գ�д����Ӧ�Ļ�ѧ����ʽ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ʮ�����ʣ���H2O �ڿ��� �� Mg �� CaO ��H2SO4 ���������� �߱���FeCl3��Һ �ఱˮ ��HNO3 ��������������ṩ�����ʣ��ش��������⣺
(1)���ڻ�������___________������ţ���ͬ��������������ʵ���_______________��
(2)����������_____��_____��ˮ��Һ�пɷ�����Ӧ�������ӷ���ʽΪH+��OH��===H2O��
(3)ʵ�����Ʊ�����Fe(OH)3�������õ�������____________����Ӧ�����ӷ���ʽΪ_____________________________________________��
(4)ʵ��������900mL 0.1mol/L����ͭ��Һ����Ҫ��ȡ�����ʣ�������������ѡȡ��������Ϊ________g�������ƺõ���Һ��ȡ��300mL�����к���SO42-����ĿΪ_______����NAΪ�����ӵ�������ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Cl2��Ӧ4HCl��Ũ��+MnO2 ![]() MnCl2+ Cl2��+2H2O������˵������ȷ����
MnCl2+ Cl2��+2H2O������˵������ȷ����
A. ��ԭ����HCl����������MnO2
B. ÿ��2molHCl��������ת�Ƶ��ӵ����ʵ���Ϊ2mol
C. ÿ����1mol MnO2����ԭ�����õ�HCl����4mol
D. ת�Ƶ��ӵ����ʵ���Ϊ1molʱ�����ɱ�״����Cl2�����Ϊ11.2L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��W��X��Y��ZΪ�������ʣ�����ͷ��ʾ��һ��ת���ij�����Ӧ�����г�������ʵ��ͼʾת����ϵ����

A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������NA��ʾ����٤��������
A. ��ӦTiO2(s) + 2Cl2(g)��TiCl4(g) + O2(g) ��H>0���Է����У���ԭ������S>0
B. ���¸����ܵ��õ�������������Լ����ܵ��ĸ�ʴ
C. ������KspMg(OH)2=5.6��1012����pH=10��Mg2+����Һ�У�c(Mg2+)��5.6��108 mol��L1
D. 1molCl2����ˮ������Һ��Cl2��HClO��ClO-��Cl-������������Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ���� 1.0 L w mol��L��1 CH3COOH ��Һ�� 0.1 mol NaOH�����ϣ���ַ�Ӧ��Ȼ������Һ�м���CH3COOH��CH3COONa����(����������¶ȱ仯)����ҺpH�ı仯��ͼ������������ȷ����
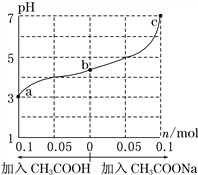
A. b����Һ��c(Na��)>c(CH3COO��)
B. ����CH3COOH������![]() ����
����
C. c����ڣ�c(CH3COOH)+c(CH3COO��) =0.1+w
D. a��b��c��Ӧ�Ļ��Һ�У�ˮ�ĵ���̶��ɴ�С��˳����c>a>b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ͪ(C3H6O)ͨ������ɫҺ�壬������ˮ���ܶ�С��1g��mL-1���е�ԼΪ55�档Ҫ��ˮ���ͪ�Ļ�����н���ͪ������������з�������Ϊ�������ǣ� ��
A.����B.��ҺC.����D.����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com