
 ȼú���ŷŴ�����CO��CO2��SO2��PM2.5������ο������ȾҲ������ȼú������أ�SO2��CO��CO2Ҳ�ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ơ��������Ż��������滷������Ч;����
ȼú���ŷŴ�����CO��CO2��SO2��PM2.5������ο������ȾҲ������ȼú������أ�SO2��CO��CO2Ҳ�ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ơ��������Ż��������滷������Ч;����| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
���� ��1��SO2�ڸ���ʧȥ����ת��ΪSO42-�����ݵ缫��Ӧʽ����д�������ش�
��2��Ӧ�ø�˹���ɽ��⣬ʼ��ץסĿ�귴Ӧ����֪��Ӧ֮��Ĺ�ϵӦ����ѧ֪ʶ���⣻
��3���ٵڶ����¶ȱȵ�һ��ߣ���Ӧ�����ʵ����ȵ�һ����룬����ƽ��ʱCO2�����ʵ����ȵ�һ���һ���٣������÷�ӦΪ���ȷ�Ӧ����������ʽ����ƽ��ʱ������ֵ����ʵ������÷�Ӧ�������������ķ�Ӧ�����������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽ����ƽ�ⳣ����
���ڷ�Ӧ�е���Ӧ������ʵ���֮�ȵ��ڻ�ѧ������֮��ʱ������Ӧ���ת������ȣ�ijһ�ַ�Ӧ��Խ�࣬��ת����Խ�ͣ�����һ�ַ�Ӧ���ת������Խ�ߣ��ݴ˴��⣻
�۸���Ũ����Qc��ƽ�ⳣ��K�Ĵ�С���жϷ�Ӧ���еķ�����ȷ�����淴Ӧ�����ʣ�
�ܵ���ѧ��Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��ٷ����仯�������ܶȺ�ƽ����Է��������Ĺ�ʽ���з��������⣮
��� �⣺��1��SO2�ڸ���ʧȥ����ת��ΪSO42-������缫��ӦΪ��SO2+2H2O-2e-=SO42-+4H+��
�ʴ�Ϊ��SO2+2H2O-2e-=SO42-+4H+��
��2��Ӧ�ø�˹���ɽ��⣬��H=-��H1-��H2+$\frac{3}{2}$��H3+2��H4=-��$\frac{3}{2}$c+2d-a-b��kJ•mol-1������CH3OH��l��ȼ���ȵ��Ȼ�ѧ����ʽΪCH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-��$\frac{3}{2}$c+2d-a-b��kJ•mol-1��
�ʴ�Ϊ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-��$\frac{3}{2}$c+2d-a-b��kJ•mol-1��
��3����ʵ��1��CO��ת����Ϊ��100%=40%��ʵ��2��CO��ת����Ϊ��100%=20%����ʵ��1��ת���ʴ���ʵ��2����˵���¶�����ƽ�����淴Ӧ�����ƶ�������Ӧ���ȣ�
ƽ��ʱCO�����ʵ���Ϊ1.6mol����
CO��g��+H2O��g��?CO2��g��+H2��g����
��ʼ��mol����2 1 0 0
�仯��mol����0.4 0.4 0.4 0.4
ƽ�⣨mol����1.6 0.6 0.4 0.4
�÷�Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������900��ʱ�÷�Ӧƽ�ⳣ��k=$\frac{0.4��0.4}{1.6��0.6}$=0.17��
�ʴ�Ϊ������0.17��
���ڷ�Ӧ�е���Ӧ������ʵ���֮�ȵ��ڻ�ѧ������֮��ʱ������Ӧ���ת������ȣ�ijһ�ַ�Ӧ��Խ�࣬��ת����Խ�ͣ�����һ�ַ�Ӧ���ת������Խ�ߣ�����ҪʹCO��ת���ʴ���ˮ��������0��$\frac{a}{b}$��1���ʴ�Ϊ��0��$\frac{a}{b}$��1��
��900��ʱ���ڴ������м���CO��H2O��CO2��H2��Ϊ1molʱ��Ũ����Qc=1��0.17=K�����Դ�ʱƽ��Ҫ�����ƶ�����V����V�����ʴ�Ϊ������
��A��CO2���ٵĻ�ѧ��Ӧ���ʺ�CO���ٵĻ�ѧ��Ӧ������ȣ�֤�����淴Ӧ������ȣ��ﵽ��ƽ�⣬����ȷ��
B����Ӧǰ������ϵ������ȣ�����������ѹǿʼ�ձ��ֲ��䣬����ѹǿ�����״̬��һ��ƽ�⣬�ʴ���
C��CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯���ǻ�ѧƽ��״̬������������ȷ��
D�������������ƽ����Է��������������������ʵ����ı�ֵ�����������ʵ��������仯�����������������ƽ����Է�������ʼ�ղ���ʱ����仯����ʱ��״̬��һ����ƽ��״̬���ʴ���
��ѡAC��
���� ���⿼���ȷ�Ӧ����ʽ����ѧƽ����㡢��ѧƽ��Ӱ�����ء���ѧƽ�ⳣ������ȣ����ؿ���ѧ����ͼ�������ݵķ���������������ע���֪ʶ�����������գ��Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ������Ҫ0.1mol/L NaOH��Һ900mL��0.5mol/L��������Һ500mL��������������Һ����������ش��������⣮
ʵ������Ҫ0.1mol/L NaOH��Һ900mL��0.5mol/L��������Һ500mL��������������Һ����������ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ͭ���仯�����ڿ�ѧ�о���ҵ�����о���������;��
ͭ���仯�����ڿ�ѧ�о���ҵ�����о���������;�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
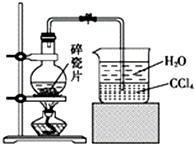 1-��������[��CH3��2CHCH2CH2Br]���л��ϳɵ���Ҫ�м��壬����������Ⱦ�ϡ������ȣ���е�Ϊ121�棬������CCl4���������촼��������������������·�Ӧ���ã���CH3��2CHCH2CH2OH+HBr$\stackrel{��}{��}$��CH3��2CHCH2CH2Br+H2O����֪���촼�ķе�Ϊ132.5�棬����ˮ��������CCl4��ʵ�����Ʊ�1-���������װ����ͼ��ʾ��
1-��������[��CH3��2CHCH2CH2Br]���л��ϳɵ���Ҫ�м��壬����������Ⱦ�ϡ������ȣ���е�Ϊ121�棬������CCl4���������촼��������������������·�Ӧ���ã���CH3��2CHCH2CH2OH+HBr$\stackrel{��}{��}$��CH3��2CHCH2CH2Br+H2O����֪���촼�ķе�Ϊ132.5�棬����ˮ��������CCl4��ʵ�����Ʊ�1-���������װ����ͼ��ʾ��| ��Ӧ�� | NaBr | 98.3% ŨH2SO4 | ���촼 | ˮ |
| ���� | 0.30mol | 35mL�������� | 0.25mol | 30mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | ��Է������� | �ܶ�/g•cm-3 | �е㣬/�� | �ܽ��/l00gˮ |
| ������ | 74 | 0.80 | 118.0 | 9 |
| ������ | 60 | 1.045 | 118.1 | ���� |
| ���������� | 116 | 0.882 | 126.1 | 0.7 |
 CH3COOCH2CH2CH2CH3+H2O��
CH3COOCH2CH2CH2CH3+H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn��ŨH2SO4 | B�� | C��ŨHNO3 | ||
| C�� | Cu��ŨHNO3 | D�� | Na2O2��NH4ClŨ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaClO��Һ��ͨ�����SO2��ClO-+SO2+H2O�THClO+HSO3- | |
| B�� | Na2SͶ��ˮ�У�S2-+2H2O?H2S+2OH- | |
| C�� | ��1molAlCl3��Һ��Ͷ��4molNa��Al3++4Na+2H2O�TAlO2-+4Na++2H2�� | |
| D�� | ��������Һ�еμ�Ba��OH��2��Һ��ǡ��ʹSO42-������ȫ��2Al3++3SO42-+3Ba2++6OH-�TAl��OH��3��+3BaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��Һ����ˮ�������c��H+��=1��10-amol•L-1����a��7ʱ�������Һ��pHһ��Ϊ14-a | |
| B�� | ��0.2mol•L-1��ijһԪ��HA��Һ��0.1mol•L-1��NaOH��Һ�������Ϻ���Һ��pH����7����Ӧ��Ļ��Һ��c��HA����c��A-�� | |
| C�� | Na2CO3��Һ��c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | ������NaHSO3��Һ��pH��7����Һ��c��SO32-����c��H2SO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ����������������Һ��Ӧ��H++OH-�TH2O | |
| B�� | ͭ����ϡ���ᷴӦ��Cu+2H+�TCu2++H2�� | |
| C�� | ������⻯����Һ��Ӧ��Cl2+2I-�TI2+2Cl- | |
| D�� | ̼������������ᷴӦ��CO32-+2H+�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com