火力发电厂燃煤排烟,释放出大量的NO
x和SO
2气体.启东大唐热电厂同时具有烟气脱氮和脱硫设施,成为高效、绿色环保燃煤电厂.试回答下列问题:
(1)脱硫:用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为生石膏(CaSO
4?2H
2O).写出上述反应的两个化学方程式:
①在空气中的SO
2与碳酸钙悬浊液反应
SO2+CaCO3=CaSO3+CO2,2CaSO3+O2+4H2O=2CaSO4?2H2O
SO2+CaCO3=CaSO3+CO2,2CaSO3+O2+4H2O=2CaSO4?2H2O
;
②在空气中的SO
2与熟石灰悬浊液反应
SO2+Ca(OH)2=CaSO3↓+H2O,2CaSO3+O2+4H2O=2CaSO4?2H2O
SO2+Ca(OH)2=CaSO3↓+H2O,2CaSO3+O2+4H2O=2CaSO4?2H2O
;
(2)脱氮:氮氧化物进入大气后,可形成硝酸型酸雨和光化学烟雾,必须对其进行处理.
①用过量的NaOH溶液吸收NO
2气体,所得的溶液中除了含有NaOH、NaNO
2,还含有
NaNO3
NaNO3
.
②若某时刻烟气排出的尾气中NO
x的含量为0.056%(体积分数),用氨气可以将其转化为无害气体,发生的反应为:6NO
x+4xNH
3=(3+2x)N
2+6xH
2O,若处理1×10
5L(标准状况)该尾气需42.5gNH
3,则x=
1.5
1.5
.
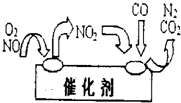
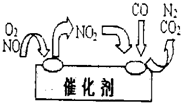
(3)汽车排出的尾气中也含有氮氧化物,为避免污染,常给汽车安装尾气净化装置.净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示.写出净化过程中的总化学反应方程式:
.

 火力发电厂燃煤排烟,释放出大量的NOx和SO2气体.启东大唐热电厂同时具有烟气脱氮和脱硫设施,成为高效、绿色环保燃煤电厂.试回答下列问题:
火力发电厂燃煤排烟,释放出大量的NOx和SO2气体.启东大唐热电厂同时具有烟气脱氮和脱硫设施,成为高效、绿色环保燃煤电厂.试回答下列问题:


 .
.
 火力发电厂燃煤排烟,释放出大量的NOx和SO2气体.启东大唐热电厂同时具有烟气脱氮和脱硫设施,成为高效、绿色环保燃煤电厂.试回答下列问题:
火力发电厂燃煤排烟,释放出大量的NOx和SO2气体.启东大唐热电厂同时具有烟气脱氮和脱硫设施,成为高效、绿色环保燃煤电厂.试回答下列问题: