
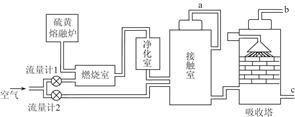
 SO2,假设SO2的体积为x,则流量计1中通入氧气的体积为1.5x,接触室中的反应为2SO2+O2
SO2,假设SO2的体积为x,则流量计1中通入氧气的体积为1.5x,接触室中的反应为2SO2+O2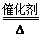 2SO3,则流量计2中通入氧气的体积为1.25x;流量计1中通入空气的体积为7.5x,流量计2中通入空气的体积为6.25x,故流经流量计1和流量计2的空气体积比应为7.5x∶6.25x=6∶5。燃烧室剩余空气6.5x,接触室剩余空气6.25x-
2SO3,则流量计2中通入氧气的体积为1.25x;流量计1中通入空气的体积为7.5x,流量计2中通入空气的体积为6.25x,故流经流量计1和流量计2的空气体积比应为7.5x∶6.25x=6∶5。燃烧室剩余空气6.5x,接触室剩余空气6.25x-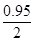 x=5.775x,剩余SO2 0.05x,故b管尾气中SO2的体积分数为0.41%;SO2可以用碱液(如氨水)吸收。③硫铁矿中铁的氧化需要消耗O2,A项正确;原料选择与SO2的转化率无关,B项错误;用硫铁矿为原料产生的废渣较多,但废气量相同,C项错误;用SO2制取SO3的过程中都需要使用催化剂,D项错误。(2)橡胶硫化所用到的为单质硫,A项错误;烷基苯磺酸钠中含有磺酸基,制取过程中需要发生磺化反应,B项正确;铅蓄电池中需要用到硫酸和硫酸铅,C项正确;过磷酸钙的制取过程中需要浓硫酸和磷矿石,D项正确。(3)SO2为酸性氧化物,可以和碱性氧化物CaO反应生成CaSO3,而CaSO3易被氧化为CaSO4。
x=5.775x,剩余SO2 0.05x,故b管尾气中SO2的体积分数为0.41%;SO2可以用碱液(如氨水)吸收。③硫铁矿中铁的氧化需要消耗O2,A项正确;原料选择与SO2的转化率无关,B项错误;用硫铁矿为原料产生的废渣较多,但废气量相同,C项错误;用SO2制取SO3的过程中都需要使用催化剂,D项错误。(2)橡胶硫化所用到的为单质硫,A项错误;烷基苯磺酸钠中含有磺酸基,制取过程中需要发生磺化反应,B项正确;铅蓄电池中需要用到硫酸和硫酸铅,C项正确;过磷酸钙的制取过程中需要浓硫酸和磷矿石,D项正确。(3)SO2为酸性氧化物,可以和碱性氧化物CaO反应生成CaSO3,而CaSO3易被氧化为CaSO4。

科目:高中化学 来源:不详 题型:单选题
| A.①②④⑦ | B.②③⑥⑦ | C.④⑤⑥⑦ | D.③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
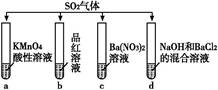
| A.试管a中实验可以证明SO2具有漂白性 |
| B.试管b中溶液褪色,说明SO2具有强氧化性 |
| C.试管c中能产生白色沉淀,说明SO2具有还原性 |
| D.试管d中能产生白色沉淀,该沉淀完全溶于稀硝酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
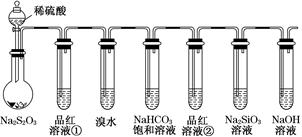
| A.若品红溶液①褪色,则说明产物中含有SO2 |
| B.若溴水褪色,则说明SO2具有还原性 |
| C.若烧瓶中产生黄色浑浊和无色气泡,则说明Na2S2O3只作氧化剂 |
| D.若品红溶液②不褪色、Na2SiO3溶液中出现白色浑浊,则说明亚硫酸比碳酸的酸性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
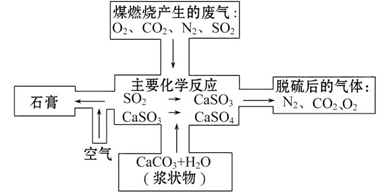
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Cu和浓硝酸 |
| B.CaO和浓氨水 |
| C.大理石和稀盐酸 |
| D.高锰酸钾溶液和浓盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
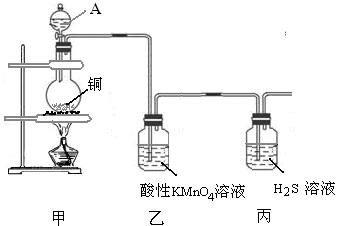
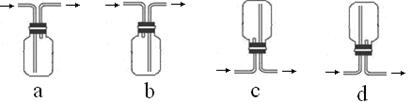
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.因浓硫酸具有强氧化性,故不可用它来干燥氢气 |
| B.浓硫酸与浓氨水靠近时产生大量白烟 |
| C.浓硫酸有强氧化性,稀硫酸不具有氧化性 |
| D.浓硫酸具有腐蚀性,取用时要小心 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com