
| A�� | S2Cl2�ĽṹʽΪCl-S-S-Cl | |
| B�� | S2Cl2��Sԭ�ӵ��ӻ�����Ϊsp2�ӻ� | |
| C�� | S2Cl2�����и�ԭ�Ӻ����������Ӿ��ﵽ8�����ȶ��ṹ | |
| D�� | S2Cl2��H2O��Ӧ�Ļ�ѧ����ʽ����Ϊ��2S2Cl2+2H2O�TSO2��+3S��+4HCl |
���� A�����ӽṹ������H2O2������S-S����S-Cl����
B�������к���2���ļ����Һ���2���µ��Ӷԣ�
C��S2Cl2�ĵ���ʽΪ 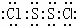 �����ݵ���ʽ�жϣ�
�����ݵ���ʽ�жϣ�
D��S2Cl2��ˮ��ˮ�⣬��������ʹƷ����ɫ�����壬��Ӧ��SԪ�ػ��ϼ۷����仯������������ԭ��Ӧ��
��� �⣺A�����ӽṹ������H2O2����H2O2�ṹ��֪������S-S����S-Cl������S2Cl2�ĽṹʽΪCl-S-S-Cl����A��ȷ��
B�������к���2���ļ����Һ���2���µ��Ӷԣ�ӦΪsp3�ӻ�����B����
C��S2Cl2�ĵ���ʽΪ 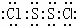 �������и�ԭ�Ӿ��ﵽ8�����ȶ��ṹ����C��ȷ��
�������и�ԭ�Ӿ��ﵽ8�����ȶ��ṹ����C��ȷ��
D��S2Cl2��ˮ��ˮ�⣬��������ʹƷ����ɫ�����壬ͬʱSԪ�ط�������������ԭ��Ӧ����ˮ�ⷴӦΪ2S2Cl2+2H2O=SO2��+3S��+4HCl����D��ȷ��
��ѡB��
���� ������S2Cl2�ĽṹΪ���壬������ӽṹ����ѧ����������ԭ��Ӧ�ȣ��ѶȲ����ǶԻ���֪ʶ���ۺ�������ѧ�������Ŀ��飬ע�����֪ʶ��ȫ�����գ���һ������������������Ŀ��


 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д� �ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
�ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
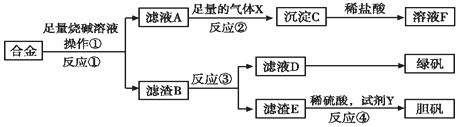
| ʵ���� | �� | �� | �� | �� |
| ϡ���������mL�� | 100 | 200 | 300 | 400 |
| ʣ�����������g�� | 9.0 | 4.8 | 0 | 0 |
| NO�����L�� | 1.12 | 2.24 | 3.36 | 4.48 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӱ뾶��W��Z��X | B�� | �����۵㣺W��Z | ||
| C�� | ������ۣ�W��X��Y��Z | D�� | ԭ��������Z��W��X��Y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
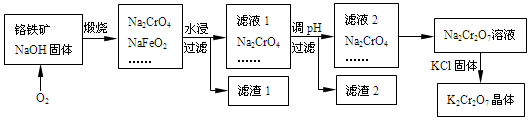
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
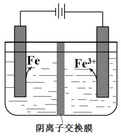
| A�� | ������Ҫ������Ӧ��Fe2++2e-�TFe | |
| B�� | �����������μ�KSCN��Һ����Һ��� | |
| C�� | ���һ��ʱ�����������pH��С | |
| D�� | ��ⷨ�Ʊ��ߴ����ܷ�Ӧ��3Fe2+$\frac{\underline{\;���\;}}{\;}$Fe+2Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֬��ˮ�ⷴӦ�ֽ�������Ӧ | |
| B�� | ����ʽΪC5H12O�Ĵ�����5�ֽṹ | |
| C�� | �Ҵ�����������Ӧ�������ᣬ������Ҵ�����ȡ����Ӧ������������ | |
| D�� | �л���ķ���ʽΪC3H6���������ϩ��C2H4����Ϊͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȩ | B�� | ��ȩ | C�� | ��ȩ | D�� | ��ȩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | �۸�/Ԫ?��-1 |
| ƯҺ����25.2%NaClO�� | 450 |
| ˫��ˮ����30%H2O2�� | 2400 |
| �ռ��98%NaOH�� | 2100 |
| �����99.5%Na2CO3�� | 600 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
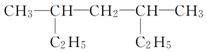 ������Ϊ��3��5-�������飮
������Ϊ��3��5-�������飮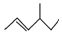 �ķ���ʽΪ��C7H14������Ϊ��4-��-2-��ϩ��
�ķ���ʽΪ��C7H14������Ϊ��4-��-2-��ϩ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com