
 已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuSO4、Fe2(SO4)3、盐酸.按要求回答下列问题:
已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuSO4、Fe2(SO4)3、盐酸.按要求回答下列问题:分析 (1)Cu、C和硫酸铁溶液构成原电池,铜易失电子发生氧化反应而作负极,碳作正极,正极上铁离子得电子发生还原反应;
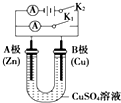
(2)①断开K2,合并K1,为原电池,B为正极,发生还原反应生成铜;
②断开K1,合并K2,B为阳极,铜为阳极生成铜离子.
解答 解:(1)铜、石墨的活泼性不同且都导电,铜和硫酸铁能自发的进行氧化还原反应,所以铜、石墨、硫酸铁溶液能构成原电池,铜易失去电子发生氧化反应,所以铜作负极,石墨作正极,负极上的电极反应式为:Cu-2e-=Cu2+,正极上铁离子得电子发生还原反应,电极反应式为2Fe3++2e-=2Fe2+,
故答案为:能;Cu-2e-=Cu2+;2Fe3++2e-=2Fe2+;
(2)①断开K2,合并K1,为原电池,B为正极,发生还原反应生成铜,电极方程式为Cu2++2e-=Cu,故答案为:Cu2++2e-=Cu;
②断开K1,合并K2,B为阳极,铜为阳极生成铜离子,电极方程式为Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+.
点评 本题综合考查原电池和电解池知识,为高频考点,侧重于学生的分析能力的考查,注意把握原电池、电解池的工作原理和电极方程式的书写,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.15mol/L | B. | 0.10mol/L | C. | 0.50mol/L | D. | 0.20mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | L与Q形成的化合物化学式为LQ | |
| B. | L、M的单质与稀盐酸反应剧烈程度:M>L | |
| C. | Q、T的氢化物在常温常压下均为无色气体 | |
| D. | M的最高价氧化物的水化物不具有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 砷的第一电离能高于磷而电负性低于磷 | |
| B. | 三氯化砷与三氯化氮分子都是三角锥构型 | |
| C. | 最高氧化物对应水化物的化学式为HAsO3 | |
| D. | 砷的第一电离能小于同周期硒的电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com