
ÖÜĘŚ Ö÷×å | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| ¶ž | ¢Ł | ¢Ś | ¢Ū | ¢Ü | |||
| Čż | ¢Ż | ¢Ž | ¢ß | ¢ą |
 £®
£®·ÖĪö øł¾Żø÷ŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆæÉÖŖ£¬¢ŁĪŖCŌŖĖŲ”¢¢ŚĪŖN”¢¢ŪĪŖO”¢¢ÜĪŖCl”¢¢ŻĪŖNa”¢¢ŽĪŖMg”¢¢ßĪŖAl”¢¢ąĪŖClŌŖĖŲ£¬½įŗĻŌŖĖŲÖÜĘŚĀÉÖŖŹ¶½ā“š£®
½ā“š ½ā£ŗøł¾Żø÷ŌŖĖŲµÄĻą¶ŌĪ»ÖĆæÉÖŖ£ŗ¢ŁĪŖCŌŖĖŲ”¢¢ŚĪŖN”¢¢ŪĪŖO”¢¢ÜĪŖF”¢¢ŻĪŖNa”¢¢ŽĪŖMg”¢¢ßĪŖAl”¢¢ąĪŖClŌŖĖŲ£¬
£Ø1£©µē×Ó²ćŌ½¶ą£¬Ąė×Ó°ė¾¶Ō½“󣬵ē×Ó²ćĻąĶ¬Ź±£¬ŗĖµēŗÉŹżŌ½“ó£¬Ō×Ó°ė¾¶Ō½Š”£¬ŌņÉĻŹöŌŖĖŲÖŠŌ×Ó°ė¾¶×ī“óµÄŹĒNa£»
·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļŌ½ĪČ¶Ø£¬·Ē½šŹōŠŌ×īĒæµÄĪŖF£¬ŌņĘųĢ¬Ēā»ÆĪļ×īĪČ¶ØµÄŹĒHF£»
ĘųĢ¬Ēā»ÆĪļĖ®ČÜŅŗ³Ź¼īŠŌµÄŹĒ°±Ęų£¬·Ö×ÓŹ½ĪŖNH3£»
½šŹōŠŌŌ½Ē棬×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®ŗĻĪļµÄ¼īŠŌŌ½Ē棬·Ē½šŹōŠŌ×īĒæµÄĪŖNa£¬Ōņ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĖįŠŌ×īĒæµÄŹĒNaOH£¬
¹Ź“š°øĪŖ£ŗNa£»HF£»NH3£»NaOH£»
£Ø2£©CO2ŹĒ¹²¼Ū»ÆŗĻĪļ£¬Ęä½į¹¹Ź½ĪŖO=C=O£¬Ģ¼Ō×ÓŗĶŃõŌ×ÓÖ®¼äÓŠ2¶Ōµē×Ó£¬Ęäµē×ÓŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©ŌŖĖŲ¢ŻŗĶ¢ß·Ö±šĪŖNa”¢Al£¬×īøß¼ŪŃõ»ÆĪļ·Ö±šĪŖNaOH”¢ĒāŃõ»ÆĀĮ£¬ĒāŃõ»ÆĀĮÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬Ąė×Ó·½³Ģ·½³ĢŹ½ĪŖ£ŗOH-+Al£ØOH£©3=AlO2-+2H2O£¬
¹Ź“š°øĪŖ£ŗOH-+Al£ØOH£©3=AlO2-+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪ»ÖĆ½į¹¹ÓėŠŌÖŹ¹ŲĻµµÄÓ¦ÓĆ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ŌŖĖŲÖÜĘŚ±ķ½į¹¹ĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚ±ķ”¢ŌŖĖŲÖÜĘŚĀɵĹŲĻµ£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 63.8 g | B£® | 53.6 g | C£® | 46.8 g | D£® | 43.2 g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 150mL1mol•L-1µÄNaClČÜŅŗ | B£® | 75mL4mol•L-1µÄNH4ClČÜŅŗ | ||
| C£® | 75mL1mol•L-1µÄFeCl3ČÜŅŗ | D£® | 150mL2mol•L-1µÄKClČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
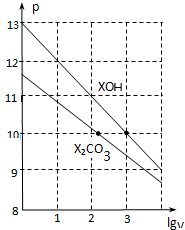
| A£® | pH=10µÄĮ½ÖÖČÜŅŗÖŠµÄc£ØX+£©£ŗXOH“óÓŚX2CO3 | |
| B£® | ŅŃÖŖ³£ĪĀĻĀ£¬0.1 mol•L-1 XHCO3ČÜŅŗµÄpH=8.31£¬ŌņKa1£ØH2CO3£©•Ka2£ØH2CO3£©£¾Kw | |
| C£® | ŅŃÖŖH2CO3µÄµēĄėĘ½ŗā³£ŹżKa1Ō¶Ō¶“óÓŚKa2£¬ŌņKa2Ō¼ĪŖ1.0”Į10-10.2 | |
| D£® | µ±lgV=2Ź±£¬ČōX2CO3ČÜŅŗÉżøßĪĀ¶Č£¬ČÜŅŗ¼īŠŌŌöĒ棬Ōņ$\frac{c£ØHC{{O}_{3}}^{-}£©}{c£ØC{{O}_{3}}^{2-}£©}$¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢õ¢ńA | ¢õ¢ņA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
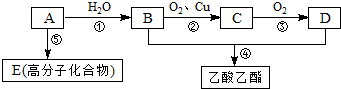
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3”¢NaHCO3Į½ÖÖŃĪµÄČÜŅŗÖŠ£¬Ąė×ÓÖÖĄą²»ĻąĶ¬ | |
| B£® | ³£ĪĀĻĀ1mol/LµÄCH3COOHČÜŅŗÓė1mol/LµÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆ»ģŗĻŅŗÖŠc £ØCH3COO-£©£¾c£ØNa+£©£¾c£ØOH-£©£¾c£ØH+£© | |
| C£® | ČÜÖŹµÄĪļÖŹµÄĮæÅضČĻąĶ¬µÄNH4ClŗĶNH4HSO4Į½ÖÖČÜŅŗÖŠ£¬c£ØNH4+£©Ē°Õߊ”ÓŚŗóÕß | |
| D£® | ³£ĪĀĻĀ£¬Ä³ČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØH+£©ĪŖ10-5mol/L£¬Ōņ“ĖČÜŅŗæÉÄÜŹĒŃĪĖį |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com