

分析 (1)依据反应物及制取气体的操作步骤分析解答,检查装置气密性后,加药顺序一般是先加入固体药品,再加入液药品,最后再加热.则依次顺序是DACB;
(2)①甲同学的方案:二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应;
②(i)依据锌粒与稀盐酸反应生成氢气进行分析解答;化学反应释放热量,气体体积具有热胀冷缩的特点.使Zn粒进入残余清液中让其发生反应.这样残余清液就可以充分反应,如果反过来,残余清液不可能全部转移到左边.若残余清液转移到左边则会残留在Y型管内壁,导致产生气体的量减少,使测定的盐酸浓度偏小;
(ii)反应完毕时,若量气管液面高于水准管液面,读取气体体积减小.
解答 解:(1)加药顺序一般是先加入固体药品,再加入液药品,最后再加热,检查装置气密性后,先加入固体,再加入液体浓盐酸,然后加热,则依次顺序是DACB,
故答案为:DACB;
(2)①与足量AgNO3溶液反应,称量生成的AgCl质量,加入足量的硝酸银溶液只能求出氯离子的量,而不能求出剩余盐酸的浓度,若以此计算氯离子增大测定结果偏大,
故答案为:偏大;
②(i)化学反应释放热量,气体体积具有热胀冷缩的特点.使Zn粒进入残余清液中让其发生反应.这样残余清液就可以充分反应,
故答案为:锌粒;残留溶液;
(ii)反应完毕,读取气体体积时,应使量气管和水准管液面相平读取,若量气管液面高于水准管液面,则读取气体体积偏小,
故答案为:偏小.
点评 本题考查了实验室制备氯气的试剂添加顺序,中和滴定的 实验操作和计算应用,实验题总体比较基础简单,注意量气管的用法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 两种情况下的正极反应都为O2+2H2O+4e-═4OH- | |
| B. | 以NaOH溶液为电解质溶液时,负极反应为Al+3OH--3e-═Al(OH)3↓ | |
| C. | 以NaOH溶液为电解质溶液时,电池工作过程中电解质溶液的碱性保持不变 | |
| D. | 电池工作时,电子通过外电路从正极流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{{ρ_1}+{ρ_2}}}{2}$ | B. | $\frac{30.0%+20.0%}{2}$ | C. | 小于25.0% | D. | 大于25.0% |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中加入稀 HCl:CO23-+2H+═H2O+CO2↑ | |
| B. | 将 NaHSO4与 Ba(OH)2溶液混合至中性:2H++SO24-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 苯酚钠溶液中通入少量 CO2气体:2C6H5O-+CO2+H2O→2C6H5OH+CO23- | |
| D. | 用惰性电极电解氯化铝溶液:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,蓄电池由化学能转化为电能 | |
| B. | 充放电时,溶液的导电能力变化不大 | |
| C. | 放电时的负极反应式为 Pb-2e-═Pb2+ | |
| D. | 充电时的阳极反应式为 Pb2++4OH-+2e-═PbO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
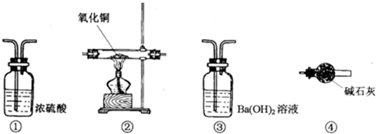
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测得氯水的pH=2;用带磨口玻璃塞的试剂瓶保存K2CO3溶液 | |
| B. | 用酸式滴定管或移液管量取20.00 mL酸性K2Cr2O7溶液 | |
| C. | 用托盘天平称取5.85 g NaNO3晶体;用10mL量筒量取6.8mL稀H2SO4 | |
| D. | 酸碱中和滴定时,滴定管和锥形瓶都需用标准液或待测液润洗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com