
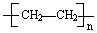 .
.分析 ①钢铁在潮湿的空气中发生吸氧腐蚀,正极发生还原反应;
②天然橡胶的成分为聚异戊二烯;
③水泥的原料是粘土和石灰石,玻璃的原料是纯碱、石灰石和石英,所以原料中均有石灰石即碳酸钙;制备玻璃的反应Na2CO3+SiO2 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2SiO3+CO2↑或CaCO3+SiO2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaSiO3+CO2↑,根据质量守恒定律书写方程式.
解答 解:①钢铁在潮湿的空气中发生吸氧腐蚀,正极氧气发生还原反应,电极反应式为:O2+4e-+2H2O=4OH-,
故答案为:O2+4e-+2H2O=4OH-;
②其中聚乙烯的结构简式为,结构简式为: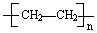 ,
,
故答案为: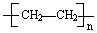 ;
;
③生产玻璃的原料是纯碱、石灰石和石英,高温下,碳酸钠、碳酸钙和二氧化硅反应分别生成硅酸钠、硅酸钙;生产水泥以黏土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;所以在玻璃工业、水泥工业中都用到的原料是石灰石,制备玻璃的反应Na2CO3+SiO2 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2SiO3+CO2↑或CaCO3+SiO2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaSiO3+CO2↑,工业上用石英砂与焦炭高温下条件下生成SiC同时生成CO,方程式为:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,
故答案为:石灰石;Na2CO3+SiO2 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2SiO3+CO2↑或CaCO3+SiO2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaSiO3+CO2↑;SiO2+3C$\frac{\underline{\;\;△\;\;}}{\;}$SiC+2CO↑.
点评 本题主要考查了化学与生活中的材料知识,平时注意基础知识的积累,注意玻璃工业、水泥工业的生产原理,题目较简单.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 任何酸与碱发生中和反应生成1molH2O的过程中,能量变化均相同 | |
| B. | 中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 | |
| C. | 若①2H2(g)+O2(g)═2H2O(g)△H=-akJ•mol-1,②2H2(g)+O2(g)═2H2O(l)△H=-bkJ•mol-1,则 a>b | |
| D. | 能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
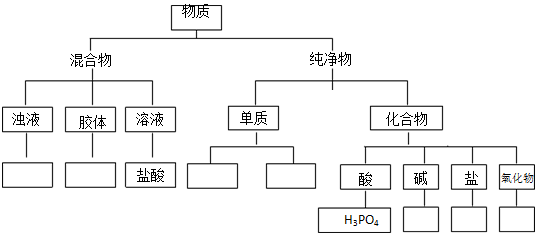
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH[H2O] | B. | CuCl2[CuSO4] | C. | NaCl[NaCl] | D. | CuSO4[Cu(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com