
��12�֣���1���������йص绯ѧ��ͼʾ�У���ȫ��ȷ����

��2�����ⱻ��Ϊ������Ԫ�ء�����ѧ�����ز����ɷ�ֹ��ȱ����������أ�KIO3���ǹ��ҹ涨��ʳ�μӵ�������ľ���Ϊ��ɫ��������ˮ������������Խ����п���⻯���������ɵ��ʵ⡣�Ե�Ϊԭ�ϣ�ͨ������Ʊ�����ص�ʵ��װ����ͼ��ʾ��

��ش��������⣺
a������ ������ɫ���������ʣ�ʵ���ҳ��� �����������ᴿ����������ɳ���ʵĹ���⡣
b�����ǰ���Ƚ�һ�����ľ��Ƶ����ڹ�������������
Һ���ܽ�ʱ������Ӧ��3I2+6KOH==5KI+KIO3+3H2O��
������Һ��������������������������Һ������������������ˮ��ȴ��
���ʱ�������Ϸ�����Ӧ�ĵ缫��ӦʽΪ ��ÿ����1mol KIO3����·��ͨ���ĵ��ӵ����ʵ���Ϊ___________________��
c���������У�Ϊȷ������Ƿ���ɣ��������Һ���Ƿ���I���������һ������
���Һ���Ƿ���I���ļ�ʵ�鷽��������Ҫ����д�±���
�ɹ�ѡ����Լ��е�����Һ��ϡ���ᣬ�Ȼ�����Һ���ƾ��ȡ��������е�һ�ֻ���־��ɡ���
|
ʵ�鷽�� |
ʵ�������� |
|
|
|
d�������ϣ��ӵ��Һ�еõ�����ؾ����ʵ��������£�
�������Һ��������Ũ�����ڡ��۹��ˡ���ϴ�ӡ��ݡ�����ؾ���
����ڵIJ��������� ������ݵIJ��������� �������ϴ��
�����Ŀ���� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� |
| �� |
| �� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����仯����֮����ת��������ʽ��ʾ���٢ڢۢ�
�����仯����֮����ת��������ʽ��ʾ���٢ڢۢ�| �� |
| �� |
| �� |
| �� |
2- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�긣��ʡ���ݸ���ѧ�߶��ڶ�ѧ����ĩ���Ի�ѧ���� ���ͣ������
�������⣩��8�֣������仯����֮����ת��������ʽ��ʾ��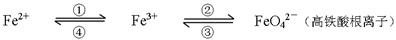
�ش������й����⣺
��1��Fe�����ϡ���ᷴӦ������ȡFeSO4�����÷�Ӧ���õ�������Һ��ʵ�������ٵ�ת����Ҫ����﴿������ѡ�õ��Լ��� ��ѡ����ţ���
A��Cl2 B��Fe C��HNO3 D��H2O2
��2������ת���õ��������������ڵ绯������ͭ���ա����������������ķ�Ӧ�Ƚϸ��ӣ�������һ��Ҫ��Ӧ��CuFeS2 + 4Fe3+ = Cu2+ + 5Fe2+ + 2S��(CuFeS2��SΪ��2��)
������˵����ȷ���� ��ѡ����ţ���
A�������ʷ���ĽǶȿ�����ͭ�����ںϽ�
B����Ӧ�У�������Ԫ�ؾ�����ԭ
C����Ӧ�У�CuFeS2����������������ԭ��
D����ת��1mol����ʱ��46 g CuFeS2�μӷ�Ӧ
��3��������Ӧ�У���FeSO4��O2��ϵ����Ϊ2 ��1������ƽ���з���ʽ��
FeSO4 + K2O2 �� K2FeO4 + K2O + K2SO4 + O2��
��4��������أ�K2FeO4����һ�����͡���Ч����ɫˮ����������ˮ�з�����Ӧ����Fe(OH)3���塣���������Ϊˮ���������ӵ�������_______��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ɽ��ʡ��̩�������ѧ����12���¿���ѧ�Ծ����������� ���ͣ������
��6�֣������仯����֮����ת��������ʽ��ʾ��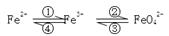
�ش������й����⣺
��1��Fe�����ϡ���ᷴӦ������ȡFeSO4�����÷�Ӧ���õ�������Һʵ�������ٵ�ת����Ҫ����﴿������ѡ�õ��Լ��� ��ѡ����ţ���
a��Cl2 b��Fe c��HNO3 d��H2O2
��2������ת���õ��������������ڵ绯������ͭ���ա����������������ķ�Ӧ�Ƚϸ��ӣ�������һ��Ҫ��Ӧ��CuFeS2+4Fe3+===Cu2++5Fe2++2S��CuFeS2��SΪ-2�ۣ���
������˵����ȷ���� ��ѡ����ţ���
a�������ʵ������������ͭ�����ںϽ�
b����Ӧ�У�������Ԫ�ؾ�����ԭ
c����Ӧ�У�CuFeS2����������������ԭ��
d����ת��1 mol e- ʱ����46 g CuFeS2�μӷ�Ӧ
��3�����������һ�����͡���Ч����ɫ��ˮ�����侻ˮԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�������и�����ѧ�����п������ۻ�ѧ�Ծ��������棩 ���ͣ������
�����仯����֮����ת��������ʽ��ʾ��

�ش������й����⣺
��1����Ԫ�������ڱ��е�λ����___________________________��
��2��Fe�����ϡ���ᷴӦ������ȡFeSO4�����÷�Ӧ���õ�������Һ��ʵ�������ٵ�ת����Ҫ����﴿������ѡ�õ��Լ���________��ѡ����ţ���
A��Cl2 B��Fe C��HNO3 D��H2O2
��3������ת���õ��������������ڵ绯������ͭ���ա����������������ķ�Ӧ�Ƚϸ��ӣ�������һ��Ҫ��ӦCuFeS2+4Fe3+��Cu2++5Fe2++2S��CuFeS2��SΪ-2�ۣ�������˵����ȷ����________��ѡ����ţ���
A�������ʷ���ĽǶȿ�����ͭ�����ںϽ�
B����Ӧ�У�������Ԫ�ؾ�����ԭ
C����Ӧ�У�CuFeS2 ����������������ԭ��
D����ת��1 mol����ʱ��46 g CuFeS2�μӷ�Ӧ
��4��������Ӧ�У���FeSO4��O2��ϵ����Ϊ2�U1������ƽ���з���ʽ��
FeSO4 + K2O2 �� K2FeO4 + K2O + K2SO4 + O2��
��5����ijϡHNO3��Fe(NO3)3�Ļ����Һ���������ۣ�������ɫ���壬 �����������������ɫ����Һ��Fe2+Ũ�Ⱥͼ���Fe�۵����ʵ���֮��Ĺ�ϵ����ͼ��ʾ��������Һ��HNO3��Fe(NO3)3�����ʵ���Ũ��֮��Ϊ__________��

��6��ijͬѧ������ˮ�������·�Ӧ��Ĺ��������ܽ��ڹ��������У�����ж�������Һ���Ƿ���Fe3+ �� ___________________________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com