
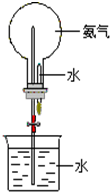
 ��֪�������Ȼ������嶼�Ǽ�������ˮ�����壬�ڱ�״����1��ˮ��������ܽ�500�����Ȼ������壬����700���İ�����
��֪�������Ȼ������嶼�Ǽ�������ˮ�����壬�ڱ�״����1��ˮ��������ܽ�500�����Ȼ������壬����700���İ��������� ��1����������ˮ���������������Һ��������谱��Ϊ1L������n=$\frac{V}{{V}_{m}}$���㰱�����ʵ������ٸ���c=$\frac{n}{V}$������Һ���ʵ���Ũ�ȣ�
��2���ٸ���n=$\frac{V}{{V}_{m}}$����HCl�����ʵ������ٸ���m=nM����HCl��������Һ����=HCl����+ˮ������������������Һ��������������
�ڸ���c=$\frac{1000�Ѧ�}{M}$������Һ���ʵ���Ũ�ȣ���Һ�Ǿ�һ�ģ�ȡ����ҺŨ����ԭ��ҺŨ����ȣ�
��� �⣺��1����������ˮ���������������Һ��������谱��Ϊ1L������Һ���Ϊ1L������°������ʵ���Ϊ$\frac{1L}{22.4L/mol}$=$\frac{1}{22.4}$mol����Һ���ʵ���Ũ��Ϊ$\frac{\frac{1}{22.4}mol}{1L}$=0.045 mol��L-1��
�ʴ�Ϊ��0.045��
��2����HCl�����ʵ���Ϊ$\frac{336L}{22.4L/mol}$=15mol��HCl����Ϊ15mol��36.5g/mol=547.5g����Һ����=1L��1000g/L+547.5g=1547.5g����Һ������������Ϊ$\frac{547.5g}{1547.5g}$��100%=35.4%��
�ʴ�Ϊ��25.4��
�ڸ���c=$\frac{1000�Ѧ�}{M}$��֪����Һ���ʵ���Ũ��Ϊ$\frac{1000��1.29��35.4%}{36.5}$mol/L=12.5mol/L����Һ�Ǿ�һ�ģ�ȡ����ҺŨ����ԭ��ҺŨ����ȣ���ȡ������Һ50mL��c��Cl-��=12.5mol/L��
�ʴ�Ϊ��12.5mol/L��
���� ���⿼����ҺŨ�ȼ��㣬�漰�������������ʵ���Ũ�ȣ�ע�����������������������ʵ���Ũ��֮���ϵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
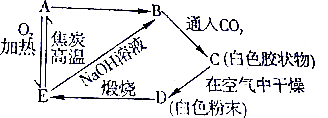
 ������������½����������������ʯ���еľ�Ʒ���������£���ʯ���ֽ���
������������½����������������ʯ���еľ�Ʒ���������£���ʯ���ֽ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | �ܵ�/�� | �е�/�� | ���� |
| CCl4 | -23 | 76 | ��TiCl4���� |
| TiCl4 | -25 | 136 | ����ʪ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ������������������ֱ���ȫȼ�գ����߷ų��������� | |
| B�� | ��H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��֪������1mol CH3COOH��ϡ��Һ�뺬1mol NaOH��ϡ��Һ��ϣ��ų�������С��57.3kJ | |
| C�� | ��C��ʯī���TC�����ʯ������H=+1.90/mol��֪�����ʯ��ʯī�ȶ� | |
| D�� | ��101 kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ2H2��g��+O2��g���T2H2O��l����H=-285.8kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol/LNa2S��Һ������S2-����С��O.1NA | |
| B�� | ��CH3COONa��Һ��CH3COO-����ĿΪNA����Na+����Ŀ����NA | |
| C�� | һ�������£�1mol N2��3 mol H2��ϳ�ַ�Ӧ��ת�Ƶĵ�����ĿΪ6NA | |
| D�� | ��״���£�11.2 L�����к��еĻ�ѧ����ĿΪ9.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̽���¶ȶԷ�Ӧ����Ӱ��ʱ���ֱ�ˮԡ���������������Һ��������Һ��һ���¶ȣ��ٽ�����Һ��� | |
| B�� | H2O2�ڹ�������ø�Ĵ��£������¶ȵ����ߣ��ֽ����ʳ����ӿ� | |
| C�� | �ü������ȼƲⶨ��Ӧ�ȣ�ʹ������ĭ���ȱ��¡����β�����������衢��ȡ�ﵽ������¶ȣ����㷴Ӧ�ȣ�ȡ2��3 �ε�ʵ��ƽ��ֵ | |
| D�� | ȡ������Ӧ��Ļ��Һ������ˮ�У��۲������ж�������Ӧ�Ƿ���ȫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com