
【题目】利用海水提取溴和镁的一般过程如下,下列说法正确的是( )
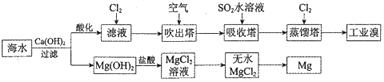
A. 工业溴中含少量Cl2,可用NaOH溶液除去
B. 工业上常利用电解MgCl2溶液冶炼金属镁
C. 富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D. 若提取1molBr2,至少需要44.8L的Cl2
【答案】C
【解析】分析:A.溴能与氢氧化钠反应;
B.根据镁是活泼的金属分析;
C.根据液溴易挥发解答;
D.根据流程图中氯气参与的反应分析计算,注意气体摩尔体积的使用条件和范围。
详解:A.由于Br2能与NaOH溶液反应,因此用NaOH溶液吸收Cl2的同时,Br2也被吸收,A错误;
B.镁是活泼的金属,工业上常用电解熔融的MgCl2冶炼金属镁,惰性电极电解MgCl2溶液生成氯气、氢气和氢氧化镁,B错误;
C.溴易挥发,因此在富集溴元素的过程中,可以使用空气吹出法,C正确;
D.溶液酸化之后得到的滤液中Br-与氯气发生反应,生成1molBr2,需要1molCl2,然后1molBr2在吹出塔富集,并在吸收塔中被SO2还原成2molBr-,然后在蒸馏塔中Cl2再次将2molBr-氧化成1molBr2,因此整个过程若提取1molBr2,至少需要2mol氯气,标准状况下为44.8 L,D错误。答案选C。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
【题目】钒和钛金属的性能都很优越,在航空航天领域用途广泛。回答下列问题:
(1)钛元素基态原子的电子排布式为______________,未成对电子数为_______________个。
(2)[TiO(H2O2)2]2+配离子呈黄色。提供中心原子孤电子对的成键原子是_____________(填元素符号),中心原子的化合价为_____________;配体之一H2O2中氧原子杂化类型为__________,H2O2分子中氧原子的价层电子对互斥模型是______________。
(3)单质钒及钛都是由______________键形成的晶体,己知金属钛是六方最密堆积,金属钒是体心立方堆积,则__________(填“钛”,或“钒”)的空间利用率较大。
(4)碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图所示。
 (小球为V原子)
(小球为V原子)
①晶胞中碳原子与钒原子的数量比为____________。
②该晶胞中与碳原子距离最近且相等的碳原子个数为_____________。
③若合金的密度为dg· cm-3,晶胞参数α=______nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A. 标准状况下,22.4 L H2O含有的分子数为NA
B. 常温常压下,1.06 g Na2CO3溶于水含有的Na+离子数为0.02 NA
C. 通常状况下,NA个CO2分子占有的体积为22.4 L
D. 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某“化学鸡尾酒”通过模拟臭虫散发的聚集信息素可高效诱捕臭虫,其中一种组分T可通过下列反应路线合成(部分反应条件略)。
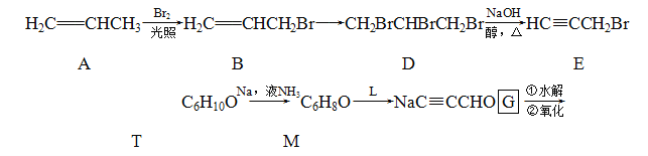
(1)A的化学名称是________,A→B新生成的官能团是________。
(2)D的核磁共振氢谱显示峰的组数为________。
(3)D→E的化学方程式为_______________________________________________。
(4)G与新制的Cu(OH)2发生反应,所得有机物的结构简式为________。
(5)L可由B与H2发生加成反应而得,已知R1CH2Br+NaC≡CR2―→R1CH2C≡CR2+NaBr,则M的结构简式为__。
(6)已知 ,则T的结构简式为________。
,则T的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池作为安全性能较好的一类化学电源得到了更快的发展,一种以联氨(N2H4)为燃料的环保电池工作原理如图所示,工作时产生稳定无污染的物质。下列说法正确的是
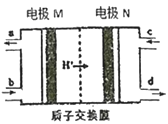
A. M极生成氮气且电极附近pH降低
B. 负极上每消耗1 mol N2H4,会有2 molH+通过质子交换膜
C. 正极的电极反应式为:O2+2H2O+4e-=4OH-
D. 电极M是原电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组同学利用如图装置研究氨气的性质。

请回答下列问题。
(1)实验室用熟石灰与氯化铵制备氨气的化学方程式是_______。
(2)下列物质能用于干燥氨气的有_____________(填字母序号)。
a. ![]() 固体 b.
固体 b. ![]() 固体
固体
c.碱石灰 d.浓![]()
(3)B中观察到的现象是_________,反应的化学方程式是_________。
(4)C中观察到的现象是__________,反应的化学方程式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用下列实验探究金属铝与铜盐溶液的反应:
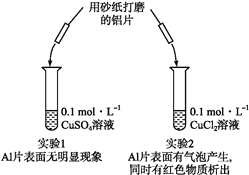
下列说法正确的是( )
A. 由实验1可以得出结论:金属铝的活泼性弱于金属铜
B. 实验2中生成红色物质的离子方程式为Al+Cu2+![]() Al3++Cu
Al3++Cu
C. 溶液中阴离子种类不同是导致实验1、2出现不同现象的原因
D. 由上述实验可推知:用砂纸打磨后的铝片分别与H+浓度均为0.2 mol·L-1的盐酸和硫酸溶液反应,后者更剧烈
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com