
【题目】①5.2g的气态乙炔(C2H2)在氧气中燃烧,生成二氧化碳和液态水,放出260kJ的热量,其热化学方程式为:___________________________________________________________。又知H2O(l)==H2O(g)△H= +44kJ/mol,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是_________kJ。
②已知:CH4 的燃烧热为890 kJ/mol,H2的热值为142.5kJg-1,现有标准状况下22.4 L CH4和H2的混合气体完全燃烧时,放出的热量为527kJ,求混合气体中CH4 和H2的体积比_____________
③将1mol NO2投入到1L容器中进行 2NO2(g)![]() N2O4(g)反应,达到平衡后将体积压缩到原来的一半再次达到平衡,则第一次平衡体系的颜色比第二次平衡的颜色_____________
N2O4(g)反应,达到平衡后将体积压缩到原来的一半再次达到平衡,则第一次平衡体系的颜色比第二次平衡的颜色_____________
【答案】C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) △H=-1300kJ/mol 628 2:3 浅
O2(g)=2CO2(g)+H2O(l) △H=-1300kJ/mol 628 2:3 浅
【解析】
①. 5.2g乙炔的物质的量为5.2g÷26g/mol=0.2mol,在氧气中燃烧生成二氧化碳和液态水,放出260kJ的热量,则1mol乙炔燃烧生成二氧化碳和液态水时放出1300kJ的热量,其热化学方程式为C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) △H=-1300kJ/mol,又知H2O(l)=H2O(g)△H= +44kJ/mol,根据盖斯定律得乙炔燃烧生成二氧化碳和气态水的热化学方程式为C2H2(g)+
O2(g)=2CO2(g)+H2O(l) △H=-1300kJ/mol,又知H2O(l)=H2O(g)△H= +44kJ/mol,根据盖斯定律得乙炔燃烧生成二氧化碳和气态水的热化学方程式为C2H2(g)+![]() O2(g)=2CO2(g)+H2O(g) △H=-1256kJ/mol,11.2L(标准状况)乙炔的物质的量为0.5mol,完全燃烧生成气态水时放出的热量是0.5mol×1256kJ/mol=628kJ,故答案为:C2H2(g)+
O2(g)=2CO2(g)+H2O(g) △H=-1256kJ/mol,11.2L(标准状况)乙炔的物质的量为0.5mol,完全燃烧生成气态水时放出的热量是0.5mol×1256kJ/mol=628kJ,故答案为:C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) △H=-1300kJ/mol;628;
O2(g)=2CO2(g)+H2O(l) △H=-1300kJ/mol;628;
②. 设混合气体中CH4 和H2的物质的量分别为a mol、b mol,H2的热值为142.5kJg-1,则H2的燃烧热为2g/mol×142.5kJ/g=285kJ/mol,列方程式为:890a+285b=527、a+b=1,解得a=0.4mol、b=0.6mol,相同条件下,气体的体积比等于物质的量之比,所以CH4 和H2的体积比为0.4:0.6=2:3,故答案为:2:3;
③.将1mol NO2投入到1L容器中进行 2NO2(g)![]() N2O4(g)反应,达到平衡后将体积压缩到原来的一半,压强增大平衡正向移动,再次达到平衡后NO2的物质的量浓度依然比原平衡大,所以第一次平衡体系的颜色比第二次平衡的颜色浅,故答案为:浅。
N2O4(g)反应,达到平衡后将体积压缩到原来的一半,压强增大平衡正向移动,再次达到平衡后NO2的物质的量浓度依然比原平衡大,所以第一次平衡体系的颜色比第二次平衡的颜色浅,故答案为:浅。


科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )

A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(s)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是
3C(g)+4D(g)反应中,表示该反应速率最快的是
A. v(A)=0.5 mol·L-1·s-1 B. v(B)=0.5 mol·L-1·s-1
C. v(C)=0.9mol·L-1·s-1 D. v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠-CO2电池的工作原理如图所示,吸收的CO2转化为Na2CO3固体和碳,沉积在多壁碳纳米管(MWCNT)电极表面,下列说法不正确的是( )
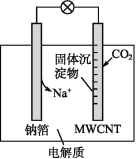
A.负极反应式为Na-e-=Na+
B.多壁碳纳米管(MWCNT)作电池的正极
C.可以用乙醇代替四甘醇二甲醚作有机溶剂
D.电池总反应式为4Na+3CO2=2Na2CO3+C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工艺流程如下:( )

已知:净化工序的目的是除去溶液中的Ca2+、Cu2+等杂质(CaF2难溶)。
下列说法不正确的是
A. 研磨矿石、适当升高温度均可提高溶浸工序中原料的浸出率
B. 除铁工序中,在加入石灰调节溶液的pH前,加入适量的软锰矿,发生的反应为MnO2+2Fe2++4H+===2Fe3++Mn2++2H2O
C. 副产品A的化学式(NH4)2S
D. 从沉锰工序中得到纯净MnCO3的操作方法是过滤、洗涤、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据:
实验编号 | 实验温度 | 试管中所加试剂及其用量 / mL | 溶液褪至无色所需时间/ min | |||
0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4溶液 | |||
① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式__________________________________________,当该反应以表中数据反应完全时转移电子数为_______________NA
(2)V1 ______
(3)根据上表中的实验①、②数据,可以得到的结论是_____。
(4)探究温度对化学反应速率的影响,应选择_____(填实验编号)
(5)该小组同学根据经验绘制了 n (Mn 2+ )随时间变化的趋势如图 1 所示,但有同学查阅已有的实验资料发现,该实验过程中 n (Mn 2+ ) 随时间变化的实际趋势如图 2 所示。

该小组同学根据图 2 所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间 / min | |||
④ | 25 | 0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4 溶液 | ||
2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||
①该小组同学提出的假设是_____。
②若该小组同学提出的假设成立,应观察到_________________________________现象。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知:四种原了最外层电子数之和为24。下列说法止确的是

A. 元索Ⅹ和元Z的最高正化合价相同
B. 单核阴离子半径的大小顺序为:r(W)>r(X)
C. 气态简单氢化物的热稳定性顺序为:Y<Z<X<W
D. 元素Z的氧化物对应水化物都是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用如图装置制备氨气并探究相关性质。

(1)装置A 中,盛有浓氨水的仪器名称为_____。装置B 的作用是_____。
(2)连接好装置并检验装置的气密性后,装入药品,然后应先_____(填 I 或Ⅱ)。
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C 中 CuO 粉末变红,D 中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为_____,该反应证明氨气具有还原性;氨与氧气的在催化剂作用下的反应也体现了这一性质,该反应化学方程式为_____。
(4)该实验缺少尾气吸收装置,如图中能用来吸收尾气的装置是_____(填装置序号)。

(5)实验室还可用如图所示装置制备氨气,化学反应方程式为_____。

(6)现将 1.92gCu 投入到一定量的浓HNO3 中,Cu 完全溶解,生成气体颜色越来越浅,共收集到标准状况下 672mL 的NOX 混合气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入标准状况下的 O2 的体积为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物的合成与结构修饰是制备具有特殊功能材料的重要过程。如图是合成具有特殊功能高分子材料W( )的流程:
)的流程:

已知:
I. ![]() R-CH2OH
R-CH2OH
II. ![]() =R2-OH
=R2-OH![]() ,R、R2、R3代表烃基
,R、R2、R3代表烃基
(1)①的反应类型是___________。
(2)②是取代反应,其化学方程式是____________________。
(3)D的核磁共振氢谱中有两组峰且面积之比是1∶3,不存在顺反异构。D的结构简式是_______。
(4)⑤的化学方程式是_________________。
(5)F的官能团名称____________________;G的结构简式是____________________。
(6)⑥的化学方程式是_________________________。
(7)符合下列条件的E的同分异构体有__________种(考虑立体异构)。
①能发生水解且能发生银镜反应 ②能与Br2的CCl4溶液发生加成反应
其中核磁共振氢谱有三个峰的结构简式是__________________。
(8)工业上也可用 合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,
合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,![]() 不易发生取代反应)
不易发生取代反应)
![]() _______________。
_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com