
反应A(g)B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
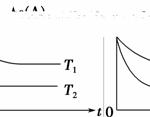
(1)上述反应的温度T1________T2,平衡常数K(T1)________K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5 min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为_______________________________________。
②反应的平衡常数K=________________________________________。
③反应在0~5 min区间的平均反应速率v(A)=________。
解析 (1)由于T2温度下达到平衡所用的时间短,根据“先拐先平,数值大”的原则,可知T1小于T2。由于T2温度下A的平衡浓度较T1温度下的小,故B、C的平衡浓度较T1温度下的大,代入平衡常数表达式可知T2时平衡常数较大。
(2)用三段式:
A(g) B(g) + C(g)
起始浓度/mol·L-1 0.050 0 0
转化浓度/mol·L-1 0.035 0.035 0.035
平衡浓度/mol·L-1 0.015 0.035 0.035
①平衡时体系总的物质的量为(0.015+0.035+0.035) mol·L-1×1.0 L=0.085 mol。
②反应的平衡常数K= =
= ≈0.082。
≈0.082。
③v(A)= =0.007 mol·L-1·min-1。
=0.007 mol·L-1·min-1。
答案 (1)小于 小于 (2)①0.085 mol ②0.082 ③0.007 mol·L-1·min-1


科目:高中化学 来源: 题型:
下列对各组物质性质的比较中,正确的是 ( )。
A.熔点:Li<Na<K
B.导电性:Ag>Cu>Al>Fe
C.密度:Na>Mg>Al
D.空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 ℃时,将0.100 mol N2O4气体充入1 L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
(1)该反应的平衡常数表达式为________;从表中分析:
c1________c2,c3________c4(填“>”、“<”或“=”)。
(2)在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为________mol·L-1·s-1。
(3)达平衡后下列条件的改变可使NO2气体浓度增大的是________(填字母序号)。
A.扩大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He
(4)若在相同条件下,起始时只充入0.080 mol NO2气体,则达到平衡时NO2气体的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是 ( )。

A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应由两步反应 A BC构成,反应过程中的能量变化曲线如图,下列叙述正确的是 ( )。

A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.加入催化剂会改变反应的焓变
D.整个反应的ΔH=E1-E2
查看答案和解析>>
科目:高中化学 来源: 题型:
图像法是研究化学反应的焓变的一种常用方法。

图1
(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化曲线如图1所示,判断下列叙述中正确的是________。
A.每生成2 mol AB时吸收 b kJ 热量
B.该反应热ΔH=+(a-b) kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键时放出a kJ能量
(2)在微生物作用的条件下,NH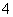 经过两步反应被氧化成NO
经过两步反应被氧化成NO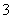 。两步反应的能量变化如图2所示:
。两步反应的能量变化如图2所示:
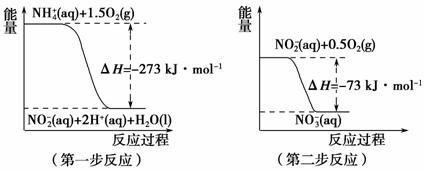
图2
1 mol NH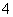 (aq)全部氧化成NO
(aq)全部氧化成NO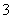 (aq)的热化学方程式是____________________________________________。
(aq)的热化学方程式是____________________________________________。
(3)图3中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素。
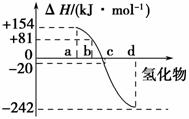
图3
①非金属元素氢化物的稳定性与氢化物生成热ΔH的关系为_______________________________________________________________。
②写出硒化氢发生分解反应的热化学方程式____________________________
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应没有涉及原电池的是 ( )。
A.生铁投入稀盐酸中
B.铜片与银片用导线连接后,同时插入FeCl3溶液中
C.纯锌投入硫酸铜溶液中
D.含铜的铝片投入浓硫酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.25 ℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA
B.1.2 g C60和石墨的混合物中,含有的碳原子数目为0.1NA
C.2.24 L N2和NH3的混合气体中,含有的共用电子对数目为0.3NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com