

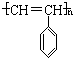
 ,故化学式为:C8nH6n,
,故化学式为:C8nH6n,

科目:高中化学 来源: 题型:
| A、该晶体中一定含有SCN- |
| B、Fe3+ 的氧化性比Br2的氧化性强 |
| C、Fe2+ 被 Br2 氧化为Fe3+ |
| D、Fe2+ 与SCN-不能形成红色的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 实验方法 |
| (1)鉴别甲烷和乙烯 | |
| (2)除去NO气体中的少量NO2 | |
| (3)除去FeCl2溶液中的少量FeCl3 | |
| (4)鉴别Na2SO4溶液和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加催化剂,v(正)和v (逆)都发生变化,且变化的倍数相等 |
| B、加压,v (正)和v (逆)都增大,且v (正)增加倍数大于v (逆)增加倍数 |
| C、降温,v (正)和v (逆)都减少,且v (正)减少倍数大于v (逆)减少倍数 |
| D、增加N2的浓度,v (正)和v (逆)都增大,且v (正)增加倍数大于v (逆)增加倍数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com