
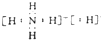 ��
������ ��1�������Ƿ����к���ȩ����������������ͭ��Һ���ȷ�Ӧ����ש��ɫ����Cu2O����ɫ�����ʵIJ���Դ�ڼ����¶ȹ��ߣ�
��2����ˮ����ɫӰ���ɫ�����Ĺ۲죬����ѡ����ȡ���ѵ���ȡ������
��3����NH5������ԭ�Ӷ��ﵽϡ��������ȶ��ṹ��˵��NH5����NH4+��H-��ɵ����ӻ����
��CuH�ܽ���ϡ�����У�CuH�е�H-ʧ���ӣ�������H+�õ��ӣ�����������Ϊ��������������Һ��2Cu+=Cu2++Cu��
�۷���������ԭ��Ӧ��������NO��ˮ�ȣ�
��4��pH=6ʱ��c��OH-��=10-8mol•L?1�����Ksp[Cu��OH��2]���㣮
��� �⣺��1����������һ�����ǻ�ȩ����������������ͭ��Һ���ȷ�Ӧ����ש��ɫ����Cu2O����������¶ȹ��ߣ�������ͭ���ȷֽ�Ϊ��ɫ������ͭ��CuO����ˮ��
�ʴ�Ϊ��ש��ɫ��CuO��
��2����ˮ���غ�ɫ��Ӱ���ɫ�����Ĺ۲죬�����ñ��ѵⵥ����ȡ���������ھƾ���ˮ������������ܣ���˲�������ȡ�����ʴ�Ϊ��B��
��3����NH5������ԭ�Ӷ��ﵽϡ��������ȶ��ṹ������ԭ�������ﵽ8�����ȶ��ṹ��������ԭ�Ӵﵽ2�����ȶ��ṹ��˵��NH5����NH4+��H-��ɵ����ӻ���������ʽΪ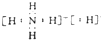 ��
��
�ʴ�Ϊ��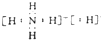 ��
��
��CuH�ܽ���ϡ�����У�CuH�е�H-ʧ����������H+�õ��ӣ�����������Ϊ������������Һ��2Cu+=Cu2++Cu�������ӷ���ʽΪ��2CuH+2H+=Cu2++Cu+2H2��
�ʴ�Ϊ��2CuH+2H+=Cu2++Cu+2H2����
��ϡ���ᱻ��ԭΪNO��ͬʱ��ˮ���ɣ�1molCuHʧȥ����2mol����NO�����ʵ���֮����3��2����ӦΪ6CuH+16HNO3=6Cu��NO3��2+3H2��+4NO��+8H2O��
�ʴ�Ϊ��6��16��6��3��4NO��8H2O��
��4��pH=6ʱ��c��OH-��=10-8mol•L?1����Ksp[Cu��OH��2]=2.2��10-20mol3•L-3��֪��c��Cu2+��=$\frac{2.2��1{0}^{-20}}{��1{0}^{-8}��^{2}}$=2.2��10-4mol•L?1���ʴ�Ϊ��2.2��10-4��
���� ���⿼����ۺϣ��漰���ʵ����ʡ�������ԭ��Ӧ��Ksp����ȣ�ע�ػ�ѧ��Ӧԭ���Ŀ��飬����ϰ���е���Ϣ��Ǩ��Ӧ������Ϊ���Ĺؼ�����Ŀ�ѶȲ���


 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2mol��ϩ���к���˫������ĿΪ0.2NA | |
| B�� | ��ϩ��1-��ϩ��ɵ�21g�����������ԭ�ӵĸ���Ϊ3NA | |
| C�� | ��״���£�11.2L���к��з��ӵ���ĿΪ0.5NA | |
| D�� | 1mol�ǻ���1mol����������������������Ϊ9NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
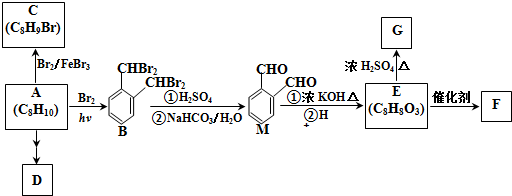

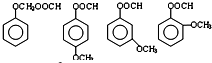
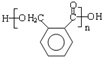 ����A����B�ķ�Ӧ�����У���ͬʱ���ɶ��ָ��������һ����B��Ϊͬ���칹�壬���ĺ˴Ź���������5�����շ壮
����A����B�ķ�Ӧ�����У���ͬʱ���ɶ��ָ��������һ����B��Ϊͬ���칹�壬���ĺ˴Ź���������5�����շ壮 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡ�ı���ˮ��Һ�еμ�����ϡ��ˮ���ȿ�����ɫ�����������ʧ����Ϊ���ɵ����屽�������ڱ�����Һ�� | |
| B�� | ��Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��CuCl2�����Һ����μ��백ˮ���ȳ�����ɫ��������ΪKSP[Mg��OH��2]��KSP[Cu��OH��2] | |
| C�� | ��������ʵ�����ģ�����������ޣ����ձ�����Ͳ�����β����������ֽ����Ӳֽ�塢�¶ȼ�������кͷ�Ӧ��Ӧ�ȵIJⶨ | |
| D�� | ��ʵ��������ϩ�ķ���װ�����ƵõIJ���ֱ��ͨ�����Ը��������Һ����Һ��ɫ��˵����ϩ�л�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� | �� | �� | �� | �� | |
| ��һ������ ��kJ/mol�� | 1681 | 1251 | 1140 | 1008 | 900 |
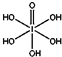 ����HIO4��ǰ��Ϊ��Ԫ�ᣬ����ΪһԪ�ᣮ��Ƚ϶�������ǿ����H5IO6��HIO4�����������������=����
����HIO4��ǰ��Ϊ��Ԫ�ᣬ����ΪһԪ�ᣮ��Ƚ϶�������ǿ����H5IO6��HIO4�����������������=����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʽΪC3H6���л���ֻ������ͬ���칹�� | |
| B�� | ��״���£�22.4 L CCl4������Ϊ154 g | |
| C�� | ѡ���ʵ��Ĵ������ȿ��Ըı仯ѧ��Ӧ���ʣ�Ҳ���Ըı䷴Ӧ���ƽ��ת���� | |
| D�� | 2 g H2��g����O2��g������ȫȼ������H2O��l���ų�����Ϊ285.8 kJ����÷�Ӧ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
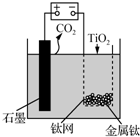 ����ͼ��ʾװ�ã�����CaF2-CaO������ʣ���ý����ƣ����øƻ�ԭTiO2�Ʊ������ѣ�����˵����ȷ���ǣ�������
����ͼ��ʾװ�ã�����CaF2-CaO������ʣ���ý����ƣ����øƻ�ԭTiO2�Ʊ������ѣ�����˵����ȷ���ǣ�������| A�� | �������У�Ca2+�������ƶ� | |
| B�� | �����ĵ缫��ӦʽΪ��C+2O2--4e-�TCO2�� | |
| C�� | ���Ʊ�������ǰ������װ����CaO���������� | |
| D�� | ����Ǧ��������װ�õĹ����Դ����+����������Pb�缫 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ������������ȼ�ϣ����������ԴΣ�� | |
| B�� | ����ȼ�յĻ�ѧ����ʽ����Ϊ4NH3+5O2$\frac{\underline{\;��ȼ\;}}{\;}$4NO+6H2O | |
| C�� | ���������״��棬��Ϊ����Һ�� | |
| D�� | �ڰ�ȼ�ϵ���У��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | ������������ | C�� | �����¶� | D�� | �������ռ���Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com