
【题目】下列说法正确的是( )
A. 含有离子键的化合物一定是离子化合物
B. 阳离子一定由金属元素组成
C. 离子化合物中一定含有金属元素
D. 非金属元素所组成的化合物中不可能含有离子键
科目:高中化学 来源: 题型:
【题目】用特殊方法把固体物质加工到纳米级(1~10nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同的数量级的是( )
A. 溶液 B. 悬浊液 C. 胶体 D. 乳浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和苯都是重要的化工原料.下图是某有机物B合成的过程. 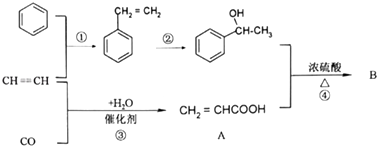
请回答:
(1)写出反应①的反应类型 , 反应②所加试剂 .
(2)关于物质A(CH2=CHCOOH)化学性质的说法正确的是 .
A.物质A含有一种官能团
B.物质A与Na2CO3溶液反应能产生气泡
C.物质A不能使酸性KMnO4溶液褪色
D.常温常压下,物质A呈气态
(3)反应④的反应机理与制取乙酸乙酯相似,写出其化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组模拟企业对含铬废水(Cr2O72﹣和Cr3+)处理流程如图1 
已知:2CrO42﹣+2H+═Cr2O72﹣+H2O
请回答:
(1)用离子方程式表示调节池里发生的反应: .
(2)操作Ⅰ得到的残渣的化学式为 .
(3)操作Ⅲ调节pH时最适合作为调节剂的是 .
A.4molL﹣1盐酸
B.6molL﹣1硫酸
C.石灰乳
D.碳酸钠
(4)为检测处理后废水中铬的含量,取100mL处理后的样品于锥形瓶中,用浓醋酸调节pH=5,并加入适量固体抗坏血酸,使Cr2O72﹣完全转化为Cr3+ , 再用amolL﹣1的EDTA(用H4Y表示)标准溶液进行滴定,其反应原理为:Cr2O72﹣→2Cr3+ , Cr3++Y4﹣=CrY﹣
①滴定时采用如图2所示的侧边自动定零位滴定管,具有的优点是 .
②实验消耗EDTA标准溶液b mL,则处理后废液中含铬浓度为mgL﹣1(用含a、b的式子表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 一般的化合反应为放热反应,所以C和CO2反应放热
B. 含有共价键的化合物一定是共价化合物
C. 所有的燃烧反应、中和反应一定是放热反应
D. 需要加热才能发生的化学反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是化学学习的工具.如图是镁元素在周期表中的表示,下列有关镁元素信息不正确的是( ) 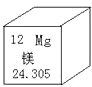
A.原子序数是12
B.它是金属元素
C.原子结构示意图为 ![]()
D.镁元素在地壳中的含量为24.305%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氧化性:Br2>Fe3+>I2 , 向含a mol FeI2的溶液中加入含b mol Br2的溴水,充分反应.下列说法不正确的是( )
A.离子的还原性强弱:I﹣>Fe2+>Br﹣
B.当a≥b时,发生的离子反应:2I﹣+Br2═I2+2Br﹣
C.当5a=4b时,反应后的离子浓度之比:c(Fe2+):c(Fe3+):c(Br﹣)=1:1:5
D.当3a≤2b时,发生的离子反应:2Fe2++2I﹣+2Br2═2Fe3++I2+4Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量Na2CO3和NaHCO3的均匀混合物分成等量的两份.将其中的一份直接加热至恒重,质量减轻了1.24g;另一份加入一定;量某浓度的盐酸至恰好反应完全,收集到标准状况下2.24L气体,消耗盐酸40.0mL.试计算:
(1)原均匀混合物中NaHCO3的物质的量.n(NaHCO3)=mol.
(2)盐酸的浓度c(HCl)=mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小 | b极有气体产生 | d极溶解 | 电流计指示在导线中 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d
B.b>c>d>a
C.d>a>b>c
D.a>b>d>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com