
已知:4NH3+5O2 4NO+6H2O,4NO+3O2+2H2O→4HNO3
4NO+6H2O,4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80.
(1)a mol NO完全转化为HNO3理论上需要氧气 mol.
(2)为使NH3恰好完全氧化为NO,氨﹣空气混合气体中氨的体积分数(用小数表示)为 (保留2位小数).
(3)20.0mol NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量硝酸,以及其他成分(高温下NO与O2不化合).计算氨转化为NO和HNO3的总转化率.
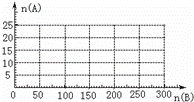
(4)20.0mol NH3和一定量空气充分反应后,再转化为硝酸.通过计算,在图中画出HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线.
考点: 化学方程式的有关计算;氮的氧化物的性质及其对环境的影响.
专题: 计算题.
分析: (1)根据一氧化氮和氧气完全转化为HNO3的关系式计算;
(2)使NH3恰好完全氧化为NO,根据氨气计算需要氧气的量,再根据体积分数公式进行计算;
(3)根据反应过程中氮气的量不变进行计算,算出生成硝酸的物质的量,再根据原子守恒计算转化率;
(4)采用极限法找出氨气、空气和硝酸的关系,并画出硝酸和空气的关系图象.
解答: 解:(1)设需要氧气的物质的量为x,
4NO+2H2O+3O2=4HNO3
4mol 3mol
amol x
x=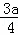 mol=0.75amol,则需要氧气的物质的量为0.75a mol,
mol=0.75amol,则需要氧气的物质的量为0.75a mol,
故答案为:0.75a;
(2)根据氨气被氧气恰好完全氧化为NO的方程式,可假设氨气的体积是4L,设需要空气的体积为y,
4NH3+5O2 4NO+6H2O
4NO+6H2O
4 5
4L 0.20y
y=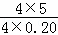 L=25L,氨﹣空气混合物中氨的体积分数=
L=25L,氨﹣空气混合物中氨的体积分数= ≈0.14,
≈0.14,
故答案为:0.14;
(3)设生成x mol HNO3,空气中氧气的体积分数为0.20,氮气的体积分数为0.80,空气中氮气的量是氧气的4倍,4(2x+18.0× +12.0)=150.0,解得:x=1.5(mol),根据氮原子守恒,NH3的转化为HNO3的转化率=
+12.0)=150.0,解得:x=1.5(mol),根据氮原子守恒,NH3的转化为HNO3的转化率= ×100%=7.5%; NH3的转化为NO的转化率=
×100%=7.5%; NH3的转化为NO的转化率=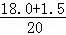 ×100%=97.5%,
×100%=97.5%,
故答案为:氨转化为NO和HNO3的转化率分别是7.5%和97.5%;
(4)4NH3+5O2 4NO+6H2O①,4NO+3O2 +2H2O=4HNO3②,将
4NO+6H2O①,4NO+3O2 +2H2O=4HNO3②,将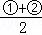 得:NH3+2O2=H2O+HNO3③,由①③知,当
得:NH3+2O2=H2O+HNO3③,由①③知,当 ≤
≤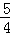 ,即
,即 ≤
≤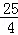 时无硝酸生成,此时20.0mol氨气所需空气量为:
时无硝酸生成,此时20.0mol氨气所需空气量为: ×20.0mol=125mol;
×20.0mol=125mol;
当 ≤
≤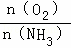 ≤
≤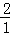 ,即
,即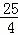 ≤
≤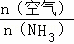 ≤
≤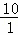 ,时有硝酸生成,此时20.0mol氨气所需空气量为10×20.0mol=200mol,生成硝酸的物质的量是20mol,所以HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线为
,时有硝酸生成,此时20.0mol氨气所需空气量为10×20.0mol=200mol,生成硝酸的物质的量是20mol,所以HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线为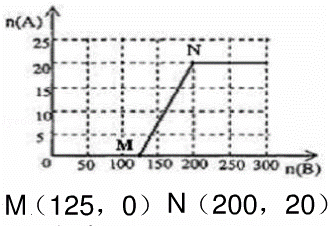 ,
,
答:HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线为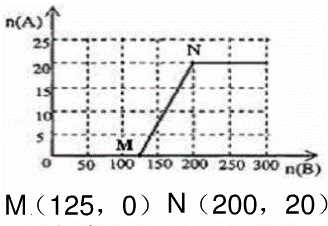 .
.
点评: 本题考查了氧化还原反应的计算,难点是计算转化率,明确氮气和氧气的关系是解本题的关键,结合原子守恒来分析解答,题目难度较大.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
已知同温同压下,下列反应的焓变和平衡常数分别表示为
H2(g)+ O2(g)=H2O(g)△H1 K1
O2(g)=H2O(g)△H1 K1
 N2(g)+O2(g)=NO2(g)△H2 K2
N2(g)+O2(g)=NO2(g)△H2 K2
 N2(g)+
N2(g)+ H2(g)=NH3(g)△H3 K3
H2(g)=NH3(g)△H3 K3
则反应2NH3(g)+ O2(g)=2NO2(g)+3H2O(g)的△H和K分别为( )
O2(g)=2NO2(g)+3H2O(g)的△H和K分别为( )
|
| A. | 2△H1+2△H2﹣2△H3 3K1+2K2﹣2K3 |
|
| B. | 2△H3﹣3△H1﹣2△H2 |
|
| C. | 3△H1+2△H2﹣2△H3 |
|
| D. | 3△H1+2△H2﹣2△H3 3K1+2K2﹣2K3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义.根据已学知识回答下列问题:
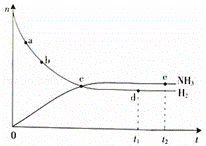
(1)对于密闭容器中的反应:N2(g)+3H2(g)═2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如右下图所示.
下列叙述正确的是 (填选项).
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大
(2)已知N2(g)+3H2 (g)═2NH3(g)△H=﹣92.4kJ•mol﹣1
①合成氨工业采取的下列措施不可用平衡移动原理解释的是 (填选项).
A.采用较高压强(20MPa~50MPa)
B.采用500℃的高温
C.用铁触媒作催化剂
D.将生成的氨液化并及时从体系中分离出来
②合成氨工业中采用了较高压强(20MPa~50MPa),而没有采用100MPa或者更大压强,试解释没有这么做的理由 .
③在容积均为2L(容器体积不可变)的甲、乙两个容器中,分别加入2molN2、6molH2和1molN2、3molH2,在相同温度、催化剂下使其反应.最终达到平衡后,两容器N2转化率分别为α甲、α乙,则甲容器中平衡常数表达式为 (用含α甲的代数式表示,化简为最简式),此时α甲 α乙(填“>”、“<”“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图:
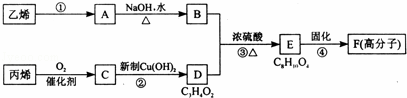
关于该过程的相关叙述正确的是( )
|
| A. | 反应④的反应类型是缩聚反应 |
|
| B. | 物质A是卤代烃 |
|
| C. | 物质B催化氧化后可以得到乙醛 |
|
| D. | 1 mol物质D最多可以消耗2 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物与生产、生活关系密切.
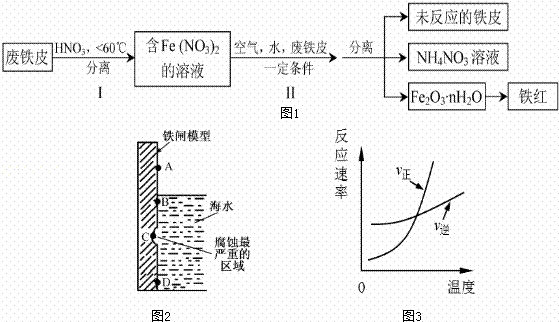
(1)如图2是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图这一腐蚀过程中发生还原反应的物质是 (填化学式).图2中A、B、C、D四个区域,生成铁锈最多的是 (填字母).
(2)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:(图1)
步骤 I若温度过高,将不利于反应的进行,用适当的文字和化学方程式进行解释: .
步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O→2Fe2O3•nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为 上述生产流程中,能体现“绿色化学”思想的是 (任写一项).
(3)已知t℃时,反应FeO(s)+CO(g)⇌Fe(s)+CO2(g)的平衡常数为K1.写出K1的表达式 .若该反应在恒容容器中反应时满足图3所示变化,则该反应的正反应为 反应(选填“吸热”或“放热”).若在t℃的2L恒温密闭容器中加入0.02mol FeO(s),并通入一定量CO.若5min后FeO(s)转化率为50%,则CO2的平均反应速率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A(化学式为C4H8O3)在一定条件下的性质有:在浓硫酸存在下,可脱水生成能使溴水褪色的只有一种结构形式的有机物B;在浓硫酸存在下,能分别与乙醇或乙酸反应生成有机物C或D;在浓硫酸存在下,还能生成分子式为C8H12O4的六元环状有机物E。则下列有关叙述一定正确的( )
A.有机物A的名称为α—羟基丁酸 B.有机物B的结构简式可能为CH3CH=CHCOOH
C.有机物C和D属同分异构体 D.环状有机物E的结构只有一种。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢化阿托醛是一种重要的化工原料,其合成路线如下:
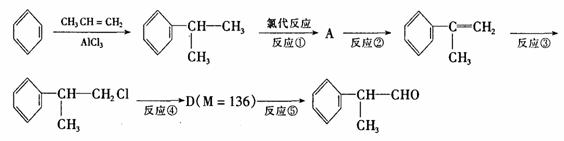
(1)氢化阿托醛被氧化后的含氧官能团的名称是 。
(2)在合成路线上②③的反应类型分别为② ③ 。
(3)反应④发生的条件是 。
(4)由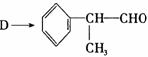 反应的化学方程式为 。
反应的化学方程式为 。
(5)1mol氢化阿托醛最多可和______mol氢气加成,1mol氢化阿托醛发生银镜反应可生成__________mol Ag。
(6)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为 。D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下RO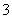 与R-发生如下反应:RO
与R-发生如下反应:RO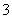 +5R-+6H+===3R2+3H2O,下列关于R的叙述中正确的是( )
+5R-+6H+===3R2+3H2O,下列关于R的叙述中正确的是( )
A.R的最外层电子数为5
B.R的氢化物的水溶液属于强酸
C.RO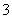 中的R只能被还原
中的R只能被还原
D.R2在常温常压下一定是气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com