
| A、与NaClO溶液混合后,溶液中c(OH-)/c(H+)变大 |
| B、加入CaCO3粉末后,溶液中c(HClO)变大 |
| C、久置后,溶液中离子种类减少 |
| D、该溶液的pH=1 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、碱性氧化物 过氧化钠 Na2O2 |
| B、碱 纯碱 Na2CO3 |
| C、金属氧化物 氧化铁 FeO |
| D、非金属氧化物 三氧化硫 SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
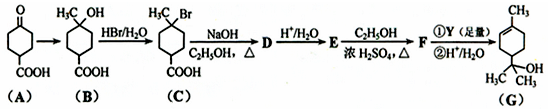
| ①R′MgBr(足量) |
| ②H+/H2O |
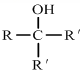
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯的结构简式:CH2CH2 |
| B、葡萄糖的结构式:C6H12O6 |
| C、1-丁烯的结构简式:CH2═CH-CH2CH3 |
| D、乙酸的实验式:C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
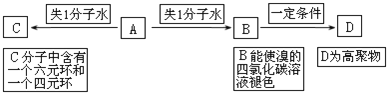
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=2的可乐中c(H+)是pH=3的柠檬水中c(H+)的10倍 |
| B、体积相同、pH相同的醋酸和盐酸完全溶解等量的镁粉,后者用时少 |
| C、pH=10的NaOH溶液与pH=12的NaOH的溶液等体积混合后,溶液的pH=11 |
| D、若V1LpH=11的NaOH溶液与V2LpH=3的HA溶液混合后显中性,则V1≤V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原合金中含0.1mol Fe、0.15mol Cu |
| B、25.4g沉淀为Cu(OH)2和Fe(OH)3的混合物 |
| C、气体X中含0.3 mol NO、0.1 mol NO2 |
| D、气体X中含0.3 mol NO2、0.1 mol NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com